Il rischio: problema di comunicazione.
La maggior parte delle donne ha difficolta a comprendere il significato del concetto “rischio”. In particolare, l’errore più comune che una donna compie è di sovrastimare l’entità del rischio personale o scambiare il rischio con causa. Questa sovrastima non è innocua perché, oltre a essere ansiogena, può condurre a comportamenti sbagliati (ad esempio pretendere più visite e un maggior numero di esami). Di conseguenza sarebbe sempre utile chiarire con la donna il significato del concetto di rischio, aiutandosi ad esempio dicendo “su 1000 donne esattamente come lei, X hanno il rischio di ammalarsi”). Numerosi sono i fattori associati ad un maggiore rischio di sviluppare un tumore al seno, la maggior parte di questi non sono modificabili. Il tumore comunque è un processo multifattoriale che necessita dell’interazione di più fattori. Il rischio è probabìlità è una misura relativa ed ha una rilevanza indiretta e non causale sullo sviluppo del tumore
Fattori di rischio più studiati
Età superiore ai 40 anni (ed in particolare età superiore ai 65 anni)
Storia personale di tumore della mammella
Mutazione di alcuni geni
Due o più parenti di I° grado con tumore diagnosticato prima dei 50anni
Densità mammaria in post-menopausa
Popolazione occidentale
Iperplasia atipica (alla micro o macrobiopsia)
Sorelle o madre con tumore della mammella
Menarca precoce (< 12 anni) Menopausa tardiva (> 55 anni)
Nulliparità
Prima gravidanza tardiva (> 30 anni)
Obesità
Scarso esercizio fisico
Dieta ricca di grassi e povera di frutta e verdura
Terapia ormonale sostitutiva protratta
Radiazioni
Fattori di rischio NON MODIFICABILI
• età: il rischio aumenta progressivamente con l’avanzare degli anni
• densità mammografica
• familiarità: tale fattore non identifica la certezza ma solo una maggiore predisposizione a sviluppare una determinata patologia oncologica. Quindi se in una famiglia sono stati riportati diversi casi di cancro, ciò non significa che altri membri si ammaleranno. È bene, però, che tali soggetti prestino maggiore attenzione, seguano stili di vita sani e si sottopongano ai test genetici, con regolarità ai programmi di screening e ai controlli suggeriti dal proprio medico
I precursori non obbligati del carcinoma della mammella
Le lesioni proliferative intraduttali sono caratterizzate da proliferazione epiteliale confinata all’unità duttolobulare e si dividono in: • iperplasia duttale usuale caratterizzata da proliferazione epiteliale solida con fenestrature irregolari con cellule e nuclei di varie dimensioni, forma ed orientamento.
Il rischio relativo di sviluppare cancro della mammella rispetto alla popolazione normale è 1,5-2. • iperplasia duttale atipica proliferazione epiteliale intraluminale con architettura cribriforme, con fenestrature (c.d. ponti romani) rigide e lumi regolari, atipie citologiche, cellule con lievi atipie citologiche e monomorfe, presenza di microcalcificazioni, delle dimensioni inferiori a 2mm. Ha un rischio relativo di sviluppare cancro della mammella rispetto alla popolazione normale è 3-5. • iperplasia colonnare atipica caratterizzata da proliferazione di epitelio colonnare dell’unità dutto-lobulare terminale con pseudo stratificazione con nuclei ovalari con ipercromasia, nucleoli evidenti, apical snout, presenza di microcalcificazioni. Ha un rischio relativo di sviluppare cancro della mammella rispetto alla popolazione normale è circa 1,5. Il carcinoma lobulare in situ di tipo classico e l’iperplasia lobulare atipica sono caratterizzati da proliferazioni epiteliali dell’unità dutto-lobulare terminale di elementi cellulari monomorfi, scarsamente coesivi, con cromatina omogenea, nucleoli non evidenti, mitosi non frequenti. Queste lesioni hanno un rischio relativo di sviluppare cancro della mammella rispetto alla popolazione normale di circa 7-10 66
Al momento attuale si parla di popolazione a rischio quando la probabilità di sviluppare un tumore per quella popolazione è maggiore rispetto ad una popolazione non esposta a quel fattore di rischio.
Ad oggi uno dei fattori di rischio più conosciuti è l’età della donna. Una donna ha una probabilità di 7,5% di sviluppare un tumore entro i 70 anni di età, in pratica una donna su 13 si potrà ammalare di carcinoma della mammella. Le donne con più di 65 anni sono ad alto rischio rispetto alle donne con meno di 40 anni.
I dati disponibili consentono di individuare dei gruppi di popolazione femminile a rischio alto (età, storia personale di tumore della mammella, mutazioni genetiche, due o più familiari diretti di 1° grado con tumore della mammella diagnosticati prima dei 50 anni, elevata densità della mammella in post-menopausa, iperplasia atipica in precedenti biopsie). L’insieme dei fattori conosciuti tuttavia non è in grado di poter spiegare gli andamenti geografici dell’incidenza di questa malattia.Sembra verosimile il ruolo forse decisivo delle abitudini alimentari della popolazione occidentale.
C’è da ritenere che la dieta favorisca l’insorgenza del tumore della mammella, sia attraverso l’uso di conservanti e l’introduzione dei cancerogeni come le amine eterocicliche che si formano nella cottura della carne, sia attraverso influenza della dieta sul metabolismo di ormoni sessuali in particolare il testosterone, e sul metabolismo dei fattori di crescita legati all’insulina. Secondo alcuni autori l’alimentazione negli USA ha fatto ampio uso di estrogeni per la loro presenza nei mangimi destinati agli animali di allevamento. A conferma di quanto detto vi è anche la correlazione tra obesità e cancro della mammella. Le analisi geografiche di incidenza e studi su animali dimostrano che la dieta ipercalorica ed iperlipidica con grassi saturi e proteine potrebbe essere un fattore di alto rischio. Studi controllati hanno inoltre dimostrato che una dieta corretta può agire a livello preventivo migliorando la prognosi e ritardando le recidive nelle donne affette da carcinoma della mammella.
Un tumore in genere origina quando i danni a carico del DNA determinano una moltiplicazione incontrollata delle cellule.L’alimentazione può influenzare l’insorgenza del tumore modificando l’ambiente interno dell’organismo che promuove ed attiva sostanze od ormoni che favoriscono il tumore e la sua progressione. Nonostante le difficoltà di affrontare sperimentazioni analitiche, data l’interazione complessa tra alimenti e metabolismo insulinico ed ormonale, è ragionevole ritenere che l’aumento del consumo di frutta, verdura, cereali integrali, legumi, e la riduzione di grassi specie saturi sia una strada percorribile a livello preventivo.
Il Fondo Mondiale per la Ricerca sul Cancro il cui compito principale è favorire la prevenzione dei tumori dopo un lungo lavoro di revisione ha stabilito delle raccomandazioni per la prevenzione alimentare del cancro
Nonostante le difficoltà di affrontare sperimentazioni analitiche, data l’interazione complessa tra alimenti e metabolismo insulinico ed ormonale, è ragionevole ritenere che l’aumento del consumo di frutta, verdura, cereali integrali, legumi, e la riduzione di grassi specie saturi sia una strada percorribile a livello preventivo.
Gli obiettivi da perseguire per una corretta alimentazione sono:
– Limitare le proteine di origine animale eccetto il pesce. Ridurre le calorie,
– Limitare il consumo di carni rosse,
– Evitare le carni conservate comprendenti ogni forma di carne in scatola, salumi, prosciutto, wurstel etc.
– Limitare il consumo di sale e di cibi sottosale,
– Limitare il consumo di alcool,
– Evitare il consumo di bevande zuccherate,
– Privilegiare cereali, legumi, frutta, verdura, pesce azzurro e olio di oliva.

Uno studio recente ha caratterizzato in modo specifico l’intensità e il tempo dedicato all’attività fisica adeguati per ottenere un calo del rischio di tumore al seno nel periodo post-menopausale. Nel 1995 sono state selezionate 118.899 donne tra i 50 e i 71 anni ed è stato loro chiesto di rammentare le abitudini all’attività fisica svolta in quattro periodi della loro vita: tra i 15 e i 18 anni, tra i 19 e i 29 anni, tra i 35 e i 39 anni e negli ultimi 10 anni. Nei 6 anni e mezzo di follow-up, successivi a queste interviste, ci sono state 4.287 nuove diagnosi di tumore al seno, di cui la maggioranza (84%) era di tipo HER-positivo. Sovrapponendo i dati è emerso che le donne che nei 10 anni precedenti l’arruolamento avevano mantenuto un livello elevato di attività fisica, da moderato a sostenuto, presentavano il 16% in meno di rischio (rischio elevato 0,84) di sviluppare la neoplasia rispetto alle donne sedentarie. L’associazione restava significativa anche con l’aggiustamento per indice di massa corporea (0,87). Tra le ragioni che possono spiegare questo legame va considerata la capacità dell’esercizio fisico di ridurre i livelli di ormoni sessuali endogeni, di modulare l’insulina e i fattori di crescita insulino-simili, di aumentare l’immunità e di ridurre lo stato infiammatorio. Tra i fattori più conosciuti il rischio è maggiore quanto più precoce è il menarca (< 12 anni) e quanto più è tardiva la menopausa (> 55 anni).
Le donne senza figli presentano un rischio maggiore di insorgenza tumorale. La protezione per le donne con figli è legata anche all’età della gravidanza; più precoce è l’età della gravidanza più la donna è protetta dal rischio di carcinoma.
La terapia ormonale sostitutiva a base di estrogeni potrebbe determinare un rischio del 20% se protratta per più di 15 anni.
Per quanto riguarda i contraccettivi orali non esistono dati che dimostrino un aumento del rischio.
Attualmente si calcola che circa il 15% dei tumori della mammella siano di tipo familiare e circa il 7 % siano ereditari.
Nelle donne appartenenti a famiglie con più casi di tumore il rischio di sviluppare un carcinoma è 3-4 volte più alto rispetto alla popolazione normale ed è più alto quanto maggiore è il grado di parentela, quanto è minore l’età di insorgenza del tumore nei familiari e se presenta bilateralità. Criteri di selezione per la consulenza genetica in donne con storia familiare sono: due o tre parenti di I° grado con carcinoma mammario o due parenti di I° grado con carcinoma ovarico o presenza di carcinoma mammario maschile. Si parla di tumore ereditario quando si riscontrano mutazioni genetiche che predispongono al carcinoma mammario.Sono stati identificati due geni denominati rispettivamente BRCA1 e BRCA2 che conferiscono suscettibilità ad ammalarsi di tumore della mammella e dell’ovaio. Il rischio di sviluppare un carcinoma per donne portatrici di mutazione BRCA1 è stimato intorno al 60%, nelle portatrici di mutazioni BRCA1 in combinazione con BRCA2 il rischio è dell’80%. Per il carcinoma ovarico tale rischio è del 20% per mutazioni BRCA1 e si dimezza per mutazioni BRCA2.
Il carcinoma ereditario si presenta di solito in età giovanile spesso è multifocale e nel 30% dei casi bilaterale.Il test genetico viene proposto dal genetista quando la probabilità di essere portatrice di una mutazione è superiore al 10%.
I criteri di selezione per una consulenza genetica in assenza di storia familiare sono:
Carcinoma mammario
Carcinoma ovarico
Carcinoma mammario bilaterale
Carcinoma mammario ed ovarico
Carcinoma mammario maschile
L’esame viene effettuato sul DNA prelevato dai linfociti del sangue circolante. Prima di intraprendere un test genetico bisognerebbe valutare gli aspetti psicologici dell’indagine e dei risultati. L’ansia per sè, per i propri familiari e la paura di progettare un futuro impone come fondamentale la consulenza psicologica, anche per una pianificazione familiare.
Nei casi di positività ai test genetici va discussa e valutata con la donna la riduzione del rischio che si pratica con tre opzioni:
– Stretta sorveglianza clinico-strumentale
– Chirurgia preventiva
– Farmacoprevenzione
Va sottolineato l’effetto cancerogeno delle radiazioni legato non solo alla dose ma anche all’età in cui vengono effettuate le indagini diagnostiche di tipo radiologico. Il rischio è più alto nella pubertà e nelle donne di età inferiore ai 20 anni, diventa trascurabile dopo i 40 anni. Bisogna quindi usare una certa cautela nel sottoporre ad esami radiologici del torace bambine e ragazze. La genetica studia i geni responsabili dei tratti ereditari, come il colore degli occhi e dei capelli, o del rischio di contrarre certi tumori. Nel tumore del seno lo studio della genetica è importante perché se c’è una storia familiare rilevante di tumori al seno e/o ovaie, si può ragionevolmente dedurre che la persona abbia ereditato un gene anormale (come BRCA 1, BRCA 2 e PALB2), correlato a un alto rischio di contrarre un tumore al seno e all’ovaio. La genomica studia invece l’interazione e le funzioni di specifici insiemi di geni e il loro ruolo nell’insorgenza di determinate patologie, come, in questo caso dei tumori del seno. Il tumore al seno è un insieme di patologie estremamente complesse, ciascuna delle quali determina alterazioni differenti, basate su caratteristiche biologiche specifiche di ciascun tumore e di ciascuna paziente. Per le donne con una diagnosi di tumore al seno può essere di grande aiuto, per orientare le domande e recepire con migliore chiarezza le risposte, poter disporre di tutte le informazioni più accurate ed esaurienti sul proprio specifico tumore. Questo inoltre può aiutare la paziente stessa a programmare, insieme al proprio medico, il miglior piano terapeutico, dopo un’attenta valutazione dei benefici sulla sopravvivenza e degli effetti collaterali delle singole terapie. Attualmente il test genomico rappresenta uno strumento utile per supportare il medico nella scelta delle opzioni di trattamento più efficace per le donne con tumore del seno in fase iniziale. Anche se genomica e genetica sembrano simili, si occupano di ambiti differenti.
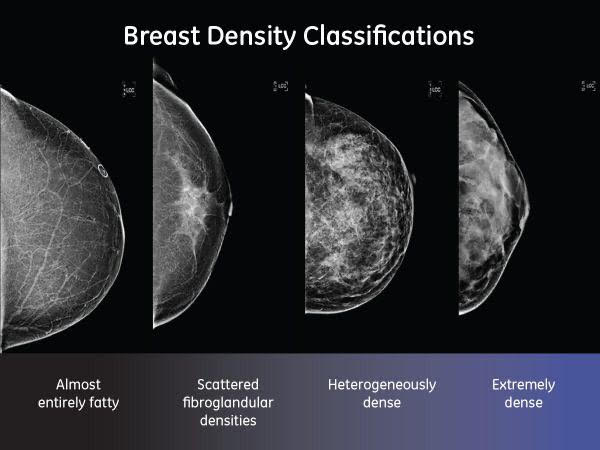
Lavori recenti introducono l’elevata densità mammaria all’esame mammografico soprattutto nelle donne in post-menopausa come fattore di rischio per il tumore della mammella.I seni densi hanno un’alta percentuale di ghiandola ed una scarsa quota di grasso. Le donne con seno a maggiore densità mammografica hanno un rischio da quattro a cinque volte più alto di sviluppare un carcinoma rispetto alle coetanee con seno non denso e quindi adiposo.
Per valutare il rischio individuale di ammalare di tumore è stato proposto da Gail un modello accettato dalla comunità scientifica.Tale modello valutando alcuni fattori stima il rischio individuale di insorgenza di carcinoma mammario.
I fattori presi in considerazione da Gail sono: l’età della donna, l’età del suo menarca, il numero di parenti con tumore della mammella, la sua età al momento della nascita del primo figlio, il numero delle eventuali biopsie al seno in presenza di iperplasie atipiche. Questo modello è stato validato a livello scientifico.Tuttavia non prende in considerazione altri fattori di rischio. Molte delle donne però considerate a rischio con questo modello non sviluppano un tumore e molte altre che non hanno i fattori compresi nel modello di Gail presentano tumori.
Pro-Tumor Inflammation (PTI) is one of the drivers of tumor survival, growth, and progression.
Multiple other cell types and cytokines are also implicated in PTI, including other interleukins, TNF-α, and macrophages.3
PTI is one of the drivers of tumor growth and suppression of immune respons
References:
1. Grivennikov SI, Greten FR, Karin M. Cell. 2010;140(6):883-899.
2. Greten FR, Grivennikov SI. Immunity. 2019;51(1):27-41.
3. Lu H, Ouyang W, Huang C. Mol Cancer Res. 2006;4(4):221-233.
4. Qian BZ, Pollard JW. Cell. 2010;141(1):39-51.