La Diagnostica Radiologica Senologica da sempre, nonostante siano trascorsi 30 anni, si basa sulla Mammografia, ovvero sulla radiografia della mammella. L’immagine mammaria nasce dalla interazione con i raggi X che l’attraversano e vanno ad impressionare la pellicola mammografia, nel caso di un sistema analogico, o un rilevatore collegato al computer, come avviene in Mammografia Digitale. Ad oggi, tuttavia, questo esame, pur mantenendo un ruolo fondamentale, deve essere integrato, oltre che con la clinica, con le altre tecniche di diagnostica per immagini, quali l’Ecografia e la Risonanza Magnetica.
La Mammografia consente di visualizzare contemporaneamente tutto il volume della mammella (esame panoramico), di identificare lesioni maligne in fase precoce, quando rappresentate unicamente da microcalcificazioni. Limiti della Mammografia sono l’utilizzo di raggi X, con conseguente rischio biologico, benché minimo, e lo studio di mammelle molto dense, ovvero con prevalente componente ghiandolare, che riduce la capacità di visualizzare le lesioni. La mammografia è un esame radiologico del seno che utilizza dosi di raggi X molto basse.
Consente di vedere se ci sono lesioni o noduli prima che siano palpabili. Per questo motivo si usa anche come screening, cioè su donne che non hanno disturbi né hanno manifestato alcun cambiamento, per identificare possibili tumori al seno in fase iniziale.
E’ consigliabile eseguire la mammografia di screening all’interno del Programma di screening organizzato, che ha un controllo di qualità e un percorso di cura già impostato nel caso siano necessari approfondimenti. Al di fuori dei Programmi di screening organizzato manca un regolare controllo da parte di terzi della qualità, per cui questa non è garantita
Come ogni intervento medico, la mammografia di screening può dare benefici ma può anche produrre danni. La mammografia non evita la comparsa del tumore al seno, ma permette di trovare tumori in fase iniziale per i quali le cure sono meno invasive e più efficaci. Il vantaggio principale è la riduzione della mortalità per tumore al seno nelle donne che partecipano al Programma di screening organizzato.
L’Ecografia della mammella è un esame complementare alla clinica ed alla Mammografia; in caso di dubbio alla palpazione o all’interpretazione del quadro mammografico consente di verificare la presenza o l’assenza di lesione e di definirne la natura liquida/solida e spesso benigna/maligna; il suo utilizzo è limitato dalla impossibilità di visualizzare contemporaneamente tutto il volume della mammella e di identificare lesioni maligne in fase precoce, quando rappresentate unicamente da microcalcificazioni; è strettamente legata all’abilità del medico che la esegue.
La Risonanza Magnetica (RM), ultima nata in diagnostica senologica, è da considerarsi esame complementare alle precedenti, spesso in grado di risolverne i limiti. Non comporta rischio biologico, ma deve essere utilizzata con precise indicazioni.
Poiché obiettivo principale della diagnostica senologica è quello di identificare il tumore maligno in fase precoce, quando non ancora palpabile e spesso di dimensioni molto piccole, Mammografia, Ecografia e Risonanza Magnetica necessitano di elevata qualità, ottenibile solo con apparecchi tecnologicamente avanzati ed adeguati, metodologie di esecuzione corrette, personale tecnico e medico ben addestrato.
Storia della mammografia: imperativi tecnologici
Punti salienti
- Il razionale alla base dello sviluppo iniziale e continuo della mammografia è la convinzione che quanto prima vengono individuati i tumori, tanto più probabile è che siano trattati in modo efficace.
- I due principali fattori trainanti nello sviluppo iniziale della mammografia furono la natura altamente letale del tumore mammario e la gravità del trattamento chirurgico disponibile all’epoca.
- La scoperta dei raggi X, nel 1895, rese possibile la visualizzazione dell’interno del corpo, che allora sembrava quasi miracolosa.
- Nel 1913, il chirurgo tedesco Albert Salomon fu il primo a individuare il tumore mammario usando i raggi X, sebbene il loro uso in ambito clinico non fosse ancora stabilito.
- Nel 1927, il chirurgo tedesco Otto Kleinschmidt pubblicò un rapporto che descrive la prima vera e propria mammografia al mondo.
- Nel 1930, il radiologo Stafford L. Warren pubblicò un articolo sull’uso di roentgenogrammi standard per la valutazione preoperatoria in vivo delle neoplasie maligne mammarie; la tecnica, tuttavia, non fu accettata diffusamente.
- Negli anni ’30 e ’40, l’avvento della dottografia o della galattografia migliorò la visualizzazione dei dotti mammari.
- Tra il 1930 e il 1950 Warren, Jacob Gershon-Cohen, un medico di Filadelfia, e il radiologo uruguaiano Raul Leborgne promossero diffusamente la mammografia come ausilio all’esame obiettivo per la diagnosi del tumore mammario.
- L’accettazione diffusa della mammografia come strumento di screening può essere attribuita al lavoro del Dott. Robert L. Egan, alla fine degli anni ’50 e durante gli anni ’60; Egan è noto come il “padre della mammografia moderna”.
- Nel 1963, il Dott. Richard H. Gold dimostrò con successo la localizzazione tramite ago di lesioni non palpabili, visibili alla mammografia, prima della biopsia.
- Negli anni ‘70 divenne popolare la xeroradiografia, una tecnica di diagnostica per immagini adattata dalla fotocopiatura xerografica, soppiantata tuttavia dall’uso della mammografia su lastra (screen-film mammography, SFM).
- La tecnica SFM utilizzata negli anni ’80 e ’90 era in grado di ottenere immagini più vivide dei tessuti mammari densi.
- Nel 1987 è stato avviato un programma di accreditamento mammografico (Mammography Accreditation Program) e dal 1992 tutti i centri mammografici statunitensi devono essere accreditati e certificati.
- Il primo rapporto sul Sistema per la refertazione e di dati della diagnostica per immagini della mammella (Breast Imaging Reporting and Data System), che ha consentito la refertazione standardizzata della mammografia, è stato pubblicato nel 1993.
- La mammografia digitale è stata introdotta alla fine del XX secolo e approvata dalla Food and Drug Administration (FDA) statunitense nel 2000.
- Con la mammografia digitale i radiologi sono in grado di manipolare il contrasto delle immagini, che consente una migliore identificazione delle masse.
- Nel 2011, la FDA statunitense ha approvato la tomosintesi mammaria digitale, che produce una ricostruzione simil-3D ottenuta da immagini di sezioni trasversali della mammella.
Imaging mammografico del tumore della mammella.
La mammografia è l’esame più efficace per la diagnosi precoce del cancro al seno, soprattutto nelle donne di età superiore ai 40 anni, la fascia di età con la più alta incidenza. Alcuni studi hanno dimostrato che la mammografia può essere particolarmente utile anche per le donne che hanno 70 anni di età ed oltre. [2, 3] Ecografia e risonanza magnetica hanno ruoli adiuvanti. Nelle pazienti più giovani, a causa della maggiore densità del seno, che può mascherare i piccoli tumori, ulteriori test come l’ecografia, l’ecografia 3D e la RM possono essere molto utili e sostitutivi della mammografia.
Tumori mammari: le calcificazioni mammografiche a stampo determinano una prognosi infausta
- Le calcificazioni a stampo (casting-type), un sottotipo di microcalcificazione, nella mammografia possono essere indicative di una prognosi peggiore nei tumori mammari (breast cancer, BCa), compresa una riduzione della sopravvivenza libera da malattia (disease-free survival, DFS) e della sopravvivenza complessiva (overall survival, OS).
Perché è importante
- La presenza di calcificazioni mammografiche a stampo è un fattore prognostico indipendente che può giustificare un trattamento più aggressivo.
Risultati principali
- L’11,8% della coorte presentava calcificazioni a stampo nella mammografia.
- Le calcificazioni a stampo erano associate con maggiore probabilità a:
- metastasi nei linfonodi ascellari rispetto ad assenza di metastasi (OR: 1,98; P=0,001);
- negatività per il recettore degli estrogeni rispetto a positività (OR: 1,49; P=0,035);
- sovraespressione del recettore del fattore di crescita dell’epidermide umano 2 (human epidermal growth factor receptor 2, HER2) rispetto a tumore HER2-negativo (OR: 2,39; P<0,001);
- tendenza a un grado istologico maggiore (G2 vs. G1; OR: 1,62; P=0,063).
- Dopo un follow-up mediano di 60 mesi, il gruppo con calcificazioni a stampo era associato a:
- DFS più breve rispetto al gruppo senza calcificazioni a stampo (78,34% vs. 90,50%; HR corretto: 1,65; P=0,024);
- OS più breve rispetto al gruppo senza calcificazioni a stampo (84,53% vs. 96,80%; HR corretto: 1,95; P=0,026).
Alcune immagini mammografiche sono riportati di seguito.
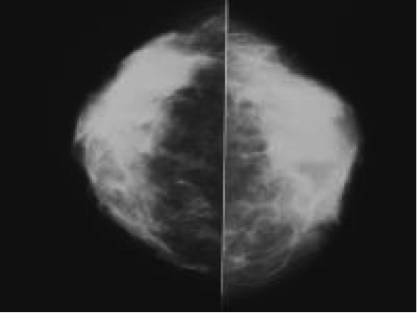
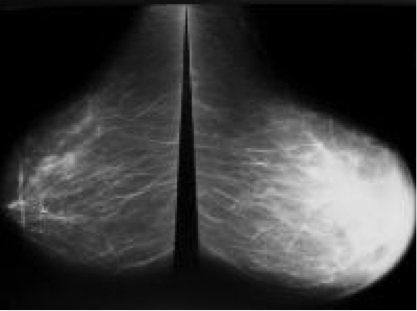
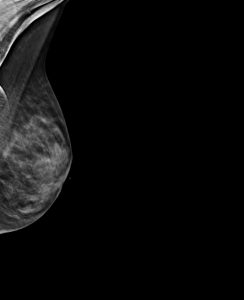
Mammografia analogica in una donna di 40 anni, mostra parenchima mammario particolarmente denso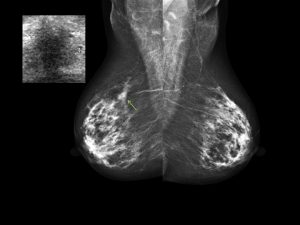
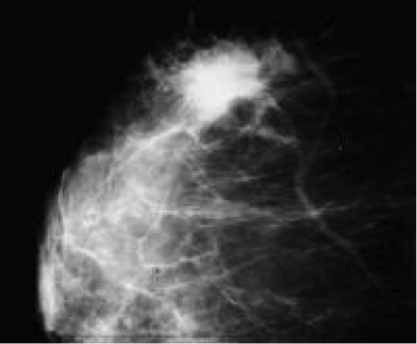
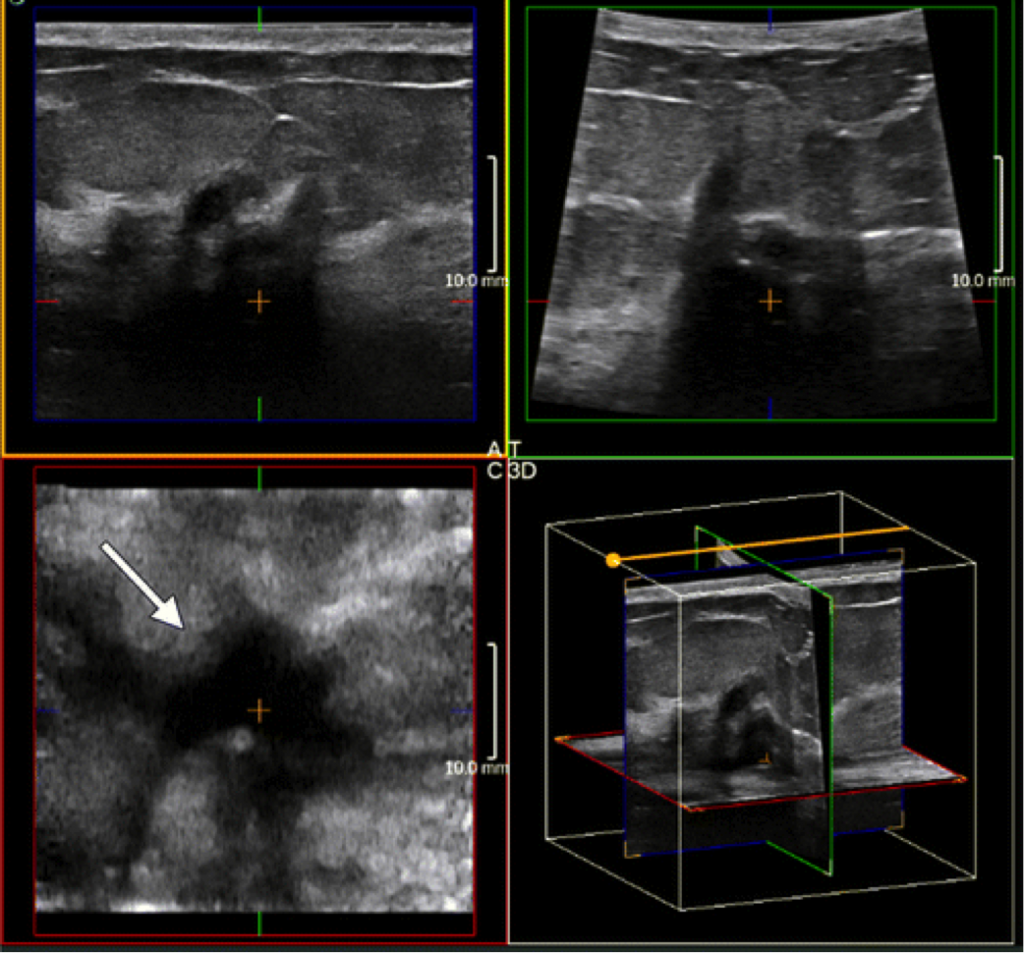
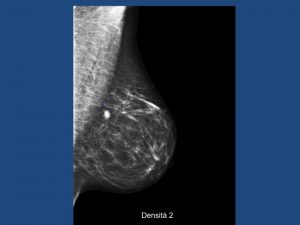
Mammografia 2d con integrazione ecografica
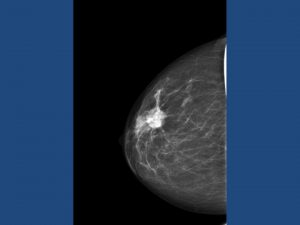
L’immagine mostra una lesione maligna
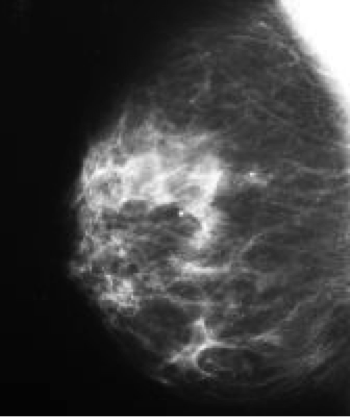
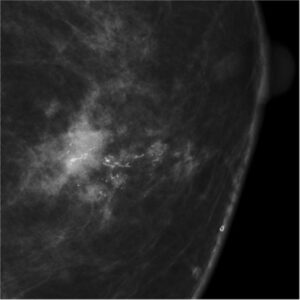
Microcalcificazioni benigne:iperplasia cistica.
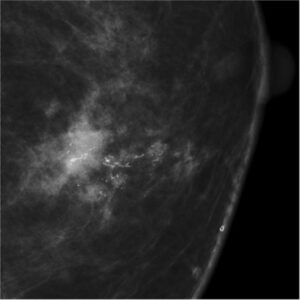
Le calcificazioni mammografiche a stampo determinano una prognosi infausta
Li Y & al.
- Le calcificazioni a stampo (casting-type), un sottotipo di microcalcificazione, nella mammografia possono essere indicative di una prognosi peggiore nei tumori mammari (breast cancer, BCa), compresa una riduzione della sopravvivenza libera da malattia (disease-free survival, DFS) e della sopravvivenza complessiva (overall survival, OS).
Perché è importante
- La presenza di calcificazioni mammografiche a stampo è un fattore prognostico indipendente che può giustificare un trattamento più aggressivo.
Disegno dello studio
- Coorte retrospettiva di 1.155 pazienti con BCa invasivo sottoposte a chirurgia mammaria definitiva.
- Finanziamento: Beijing Natural Science Foundation; altri.
Risultati principali
- L’11,8% della coorte presentava calcificazioni a stampo nella mammografia.
- Le calcificazioni a stampo erano associate con maggiore probabilità a:
- metastasi nei linfonodi ascellari rispetto ad assenza di metastasi (OR: 1,98; P=0,001);
- negatività per il recettore degli estrogeni rispetto a positività (OR: 1,49; P=0,035);
- sovraespressione del recettore del fattore di crescita dell’epidermide umano 2 (human epidermal growth factor receptor 2, HER2) rispetto a tumore HER2-negativo (OR: 2,39; P<0,001);
- tendenza a un grado istologico maggiore (G2 vs. G1; OR: 1,62; P=0,063).
- Dopo un follow-up mediano di 60 mesi, il gruppo con calcificazioni a stampo era associato a:
- DFS più breve rispetto al gruppo senza calcificazioni a stampo (78,34% vs. 90,50%; HR corretto: 1,65; P=0,024);
- OS più breve rispetto al gruppo senza calcificazioni a stampo (84,53% vs. 96,80%; HR corretto: 1,95; P=0,026).
La mammografia bilaterale mostra un carcinoma infiammatorio diffuso della mammella sinistra
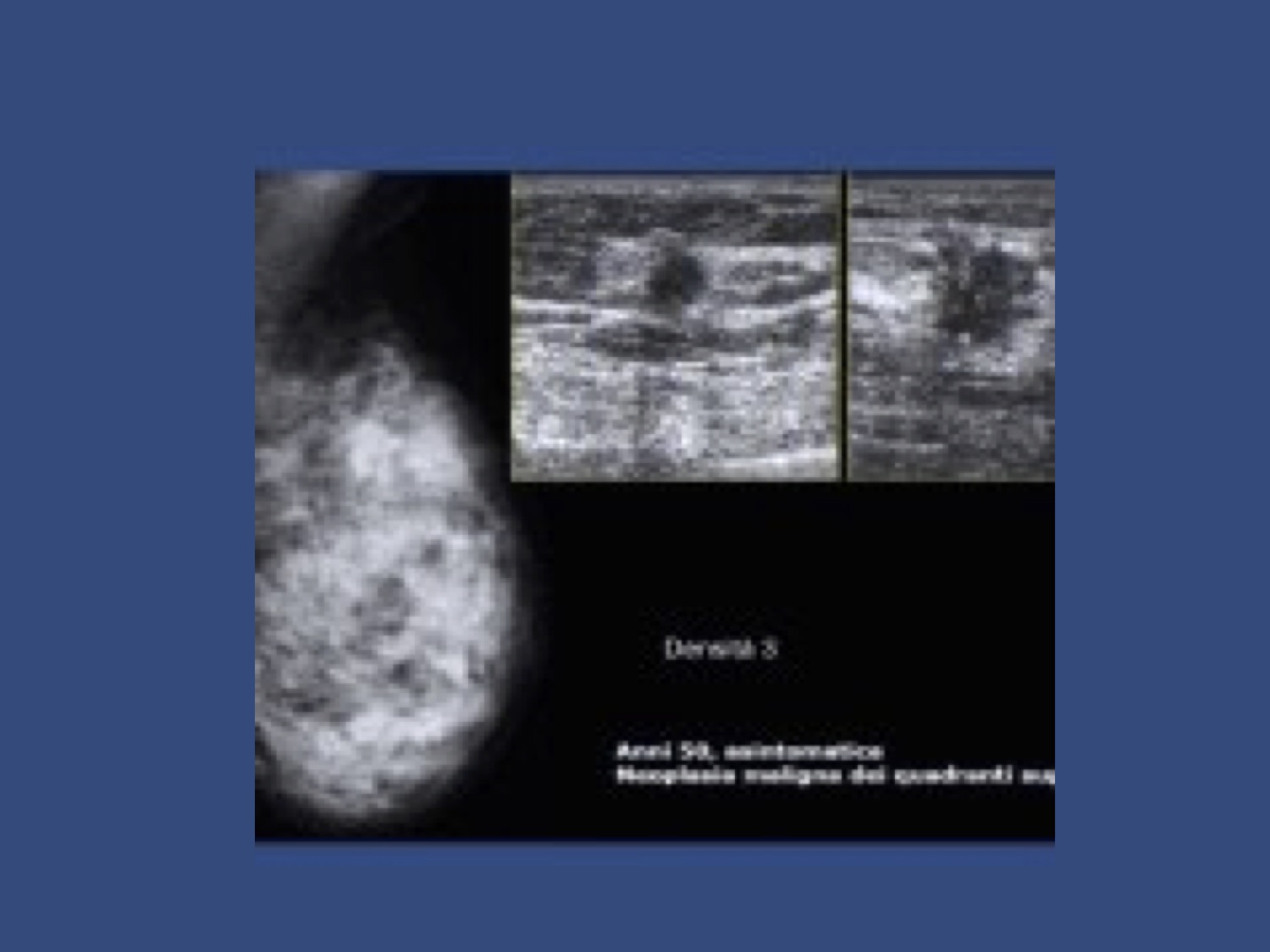
Seno denso, l’ecografia evidenzia il processo tumorale
Screening mammografico
Ci sono 2 tipi di esami mammografici; di screening e clinici. Lo screening mammografico è utilizzato in donne asintomatiche. La diagnosi precoce di piccoli tumori al seno mediante screening mammografico migliora notevolmente le probabilità di una donna di successo del trattamento. La mammografia di screening è consigliata ogni 1-2 anni per le donne, una volta che raggiungono i 40 anni di età e ogni anno una volta che raggiungono i 50 anni di età. In alcuni casi, i medici possono raccomandare di iniziare lo screening mammografico prima dei 40 anni (ad esempio, se la donna ha una forte storia familiare di cancro al seno). Gli studi hanno dimostrato che le mammografie eseguite con regolarità possono diminuire la mortalità anche nelle donne in età avanzata. [2, 3]
Gli studi hanno anche dimostrato che lo screening mammografico non dovrebbe essere basato solo su età e storia familiare di cancro al seno, ma anche sulla densità del seno, storia di biopsia mammaria pregressa, e la conoscenza sul bilancio costi-benefici dello screening. [7]
La mammografia diagnostica è eseguita nelle donne sintomatiche , in presenza di nodulo al seno o per secrezione ematica evidenziata durante l’auto-esame o una anomalia viene rilevata durante lo screening mammografico. La mammografia diagnostica richiede più tempo di una mammografia di screening e viene utilizzata per determinare la dimensione esatta, la posizione del reperto nel seno e per lo studio dei linfonodi circostanti. Tipicamente, diverse proiezioni aggiuntive del seno vengono praticate e interpretate durante la mammografia diagnostica. Così, la mammografia diagnostica è più costosa della mammografia di screening. Le donne con protesi al seno o una storia personale di cancro al seno di solito richiedono esami complementari, quali l’ecografia, utilizzata ad integrazione della mammografia diagnostica.
Per la mammografia di screening, ciascuna mammella viene esposta separatamente, in genere sia in cranio-caudale (CC) e medio-laterale-obliqua (MLO) . Per la mammografia diagnostica, ciascuna mammella viene esposta separatamente in CC, MLO, e proiezioni supplementari sulla base del problema specifico. Queste proiezioni supplementari possono includere latero-mediale (LM) e medio-laterale (ML) , ingrandimento, spot, e altri. Marker cutanei speciali sono a volte utilizzati per identificare alcune lesioni, anomalie cutanee, il capezzolo, e altre aree.
La compressione del seno è necessaria per appiattire il seno in modo che la quantità massima di tessuto possa essere esaminata. Permette anche di ridurre la dose di raggi X e immobilizzando il seno si può ridurre la sfocatura di movimento. La compressione riduce anche la dispersione di raggi X, che può degradare l’immagine.La compressione del seno può causare qualche disagio, ma non dovrebbe causare alcun dolore significativo.
Interpretazione delle Mammografie
La qualità delle mammografie dovrebbe essere valutata e, se non ottimale, gli esami dovrebbero esere ripetuti. Le mammografie di destra e di sinistra vanno analizzate back to back (in modo speculare) con le proiezioni comparabili.L’illuminazione deve essere omogenea, e adeguate condizioni di osservazione dovrebbe essere mantenute. Le mammografie vengono ispezionate con attenzione. La ricerca viene effettuata sistematicamente attraverso aree simili in entrambi i seni.
In primo luogo vanno osservate, la simmetria del seno, le dimensioni, la densità generale, e la distribuzione ghiandolare Successivamente, viene eseguita la ricerca di noduli, densità, calcificazioni, distorsioni ghiandolari e reperti associati. Per i noduli; la forma, i margini, e la densità vengono analizzati. Le lesioni maligne tendono ad avere margini irregolari e (di solito) spiculati. Le neoplasie, specialmente i cancri scirrosi, tendono ad avere densità superiore a quella del normale tessuto mammario. Bassissima densità, è documentata nelle lesioni benigne (ad esempio, cisti, lipomi, galattoceli, amartomi).
Le calcificazioni benigne sono di solito più grandi delle calcificazioni associate a malignità. Di solito sono più grossolane, spesso con margini lisci, e più facilmente visibili. Le calcificazioni benigne tendono ad avere forme specifiche: calcificazioni a guscio d’uovo in pareti delle cisti, nelle pareti arteriose, tipo popcorn in fibroadenomi, grandi e con possibili ramificazioni nei condotti ectasici, e piccole calcificazioni con un centro lucente nella cute. Le calcificazioni associate a malignità sono generalmente piccole (<0,5 mm) e spesso richiedono l’uso di una lente di ingrandimento per vederle bene. Esse tendono ad avere una forma pleomorfica o eterogenea o granulare, lineare fine, o una forma vermiculare con diramazioni (casting). La distribuzione della calcificazioni deve essere specificata come raggruppati (cluster), lineare, segmentale, regionale o diffusa.
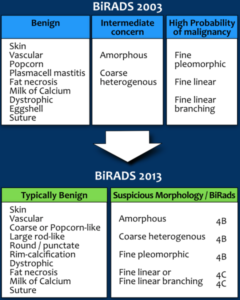
I risultati potranno riscontrare segni particolari, come ad esempio una densità lineare che potrebbe rappresentare un condotto pieno di secrezioni o forma reniforme di linfonodi intramammari (con centro radiotrasparente).I quadri associati vengono quindi presi in considerazione. Questi includono la retrazione cutanea o del capezzolo, l’ispessimento della pelle (che può essere focale o diffuso),l’ispessimento trabecolare, le lesioni cutanee, l’adenopatia ascellare, e la distorsione ghiandolare.
Per la localizzazione della lesione si utilizza uno dei quadranti, interno o esterno, inferiore o superiore. Può anche essere centrale o retroareolare. La lesione può essere descritta considerando la posizione come fosse un quadrante dell’orologio. Il seno è visto come il quadrante di un orologio con il paziente rivolto verso l’osservatore. La profondità della lesione è descritta come anteriore, media o terzo posteriore del seno. Se i risultati degli esami precedenti sono disponibili, il loro confronto è utile per valutare i cambiamenti. Tutti questi risultati sono considerati insieme, negli Stati Uniti nelle conclusioni finali è assegnata una categoria BI-RADS .
Quali sono i limiti della mammografia?
La mammografia, come tutte le tecniche diagnostiche, ha limiti legati alla metodica stessa, ai macchinari, nel 91% obsoleti, alle difficoltà di interpretazione delle caratteristiche del tessuto della mammella o perché la lesione è talmente piccola da non essere riconoscibile. La densità mammografica è la vera criticità della diagnosi precoce.
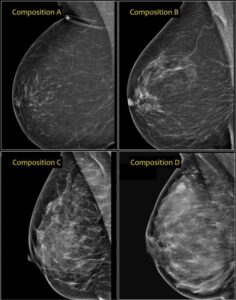
BREAST TISSUE ASSESSMENT secondo ACR BI-RADS
a. The breasts are almost entirely fatty
b. There are scattered areas of fibroglandular density
c. The breasts are heterogeneously dense, which may obscure detection of small masses
d. The breasts are extremely dense, which lowers the sensitivity of mammography A
LIMITI della MAMMOGRAFIA
mammelle opache, ghiandolari,
● sede marginale del tumore,
● scarsa densità (opacità) intrinseca del tumore,
● tumore molto piccolo,
● contorni regolari di alcuni tumori,
● difetti di apparecchiature e di esecuzione dell’esame.
Nonostante la mammografia sia considerata la tecnica principale di diagnosi precoce gli studi indicano una percentuale non trascurabile di falsi negativi oscillante dal 10 al 30 %. E’ noto che la densità mammaria rappresenta il maggior limite alla capacità della mammografia di evidenziare neoplasie precoci a causa della perdita di sensibilità legata alla sovrapposizione in immagine di diversi spessori mammari. L’avvento della modalità digitale, contrariamente alle aspettative iniziali, non ha ovviato a tale limite; tecniche più evolute nel campo dell’imaging mammografico digitale, quali la tomosintesi, mostrano forti potenzialità in questo senso.
Mammografia Postoperatoria
Le donne che hanno avuto un precedente intervento chirurgico per cancro al seno possono presentare cancro al seno con la mammografia di screening. Se una donna ha avuto una mastectomia totale, l’altro seno richiede ogni anno un follow-up perché lei è ancora a più alto rischio di sviluppare il cancro al seno . Se avesse mastectomia sottocutanea o mastectomia parziale o mastectomia parziale, richiede la mammografia di follow-up. La prima mammografia è meglio eseguirla sei mesi dopo l’intervento per fornire una base per i nuovi cambiamenti postoperatori e radioterapeutici. Successivamente, la mammografia può essere eseguita ogni 6-12 mesi per lo screening e il follow-up.
Le donne con seni trattati con impianti protesici possono essere una sfida speciale. Speciali 4-view mammografie possono essere effettuate per valutare il seno, l’impianto deve essere tirato da parte in modo che il tessuto mammario sottostante possa essere esposto. MRI può essere particolarmente utile per rilevare il cancro al seno e silicio impianto rottura in questo gruppo di pazienti.
Falsi positivi e falsi negativi
Possono verificarsi risultati falsi-positivi quando le microcalcificazioni benigne sono considerate maligne. La sommazione tessutale può apparire come una distorsione del parenchima , che può essere erroneamente definita tessuto maligno.Una lesione benigna circoscritta può mostrare segni suggestivi di malignità, insieme ad altri reperti, come ad esempio un bordo irregolare o lubulato. Secondo i dati del Breast Cancer Detection Demonstration Project, il tasso di falsi negativi della mammografia è di circa il 8-10%.A nostro giudizio il 30% di cancri d’intervallo rende più verosimile che il tasso dei falsi negativi sia più alto. Circa il 1-3% delle donne con un’anomalia clinicamente sospetta, una mammografia negativa, e un’ecografia negativa può avere il cancro al seno.
Le possibili cause di tumori al seno non diagnosticati sono: parenchima denso che oscura la lesione, cattivo posizionamento o tecnica errata, errore di percezione, errata interpretazione di una presenza sospetta, caratteristiche lievi di malignità, e la lenta crescita di una lesione. Birdwell et al hanno condotto uno studio multicentrico e hanno scoperto che, nelle mammografie precedenti con tumori senza risposta, il 30% delle lesioni erano calcificazioni, con il 17% dei 49 cluster o pleomorfo. Circa il 70% erano lesioni nodulari, con il 40% spiculati o irregolari. Per le calcificazioni e le masse, le ragioni più frequentemente suggerite per un eventuale sottodiagnosi erano i seni densi (34%) . [8] Alcuni tipi di cancro (ad esempio, carcinomi mucinosi) possono avere margini ben definiti e caratteristiche mammografiche suggestive di benignità.
Altri usi della radiografia nel cancro al seno
Un ductogramma, o galattografia, a volte è utile per determinare la causa della secrezione dal capezzolo. In questa procedura una piccola quantità di mezzo di contrasto viene iniettato all’interno di un dotto del capezzolo per delineare la forma del condotto su un’immagine radiografia e mostra se una massa è presente all’interno del condotto.
Conclusioni
- La mammografia di screening offre la possibilità di evitare il cancro al seno, ma comporta il rischio di risultati falsi-positivi, con sovradiagnosi di cancro al seno e trattamenti inutili. Welch e Passow hanno cercato di quantificare i rischi e i benefici della mammografia di screening in modo che rischi e benefici possano essere condivisi con le donne per aiutarle a prendere decisioni informate.
- Tre esiti legati alla mammografia di screening sono stati valutati per le donne con inizio mammografia all’età di 40, 50 e 60 anni: (1) riduzione dei decessi per cancro della mammella; (2) falsi positivi(comprese biopsie successive); e (3) sulla sovradiagnosi e sul sovratrattamento. Questi risultati sono riportati in termini di 1000 donne screenate annualmente per un periodo di 10 anni. A causa della variabilità e incertezza statistica, così come l’eterogeneità delle popolazioni studiate, i risultati sono riportati in una gamma dei limiti inferiori e superiori per ogni risultato.
- I dati sono stati ottenuti da studi clinici randomizzati di mammografia di screening. La riduzione dei decessi per cancro al seno, la misurazione del tasso di mortalità è stata effettuata 5 anni oltre i primi 10 anni, sulla base del presupposto che una riduzione della mortalità si estende per 15 anni dall’avvio dello screening. I risultati falsi-positivi sono stati classificati come un richiamo per ulteriori test o una raccomandazione di biopsia. Questi sono i risultati per i singoli gruppi di età:
- Su 1000 donne di40 anni, sottoposte a mammografia annua per 10 anni:
- • Tra 1 e 16 donne eviterà di morire per cancro al seno;
- • Tra 510 e 690 avranno almeno 1 test falso positivo, con 60-80 biopsie;
- • Fino a 11 donne subiranno sovradiagnosi e sovratrattamenti e trattate inutilmente con chirurgia, radioterapia o chemioterapia.
- Su 1000 donne di 50 anni, sottoposte a mammografia annua per 10 anni:
- • Tra 3 e 32 donne eviterà morire per cancro al seno;
- • Tra il 490 e 670 avranno almeno 1 test falso positivo, con 70-100 che subiranno una biopsia;
- • Tra 3 e 14 andranno incontro a sovradiagnosi e trattate inutilmente con chirurgia, radioterapia o chemioterapia.
- Su 1000 donne di 60 anni di età, sottoposte a mammografia annua per 10 anni:
- • Tra 5 e 49 donne eviterà la morte per cancro al seno;
- • Tra 390 e 540 avranno almeno 1 test falsio positivo, con 50-70 che subiranno una biopsia;
- • Tra 6 e 20 andranno incontro a sovradiagnosi e sovratrattamento,e trattate inutilmente con chirurgia, chemioterapia o radieterapia.
TOMOSINTESI
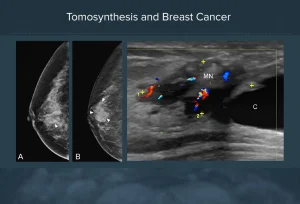
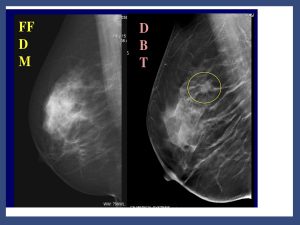
E’ indubbio che il modo più naturale ed efficace per rimuovere il cosiddetto rumore strutturale in mammografia consista nel separare fisicamente le varie strutture anatomiche del seno. La mammografia rappresenta infatti una proiezione bidimensionale di una struttura tridimensionale per cui, geometricamente, tessuti appartenenti a piani diversi risultano sovrapposti nell’immagine radiografica. Non c’è nulla di nuovo in tutto ciò, semplicemente la tecnologia tomografica ha raggiunto la maturità anche per la diagnosi precoce del tumore al seno per cui sistemi dedicati sono in fase di applicazione clinica.
La tomosintesi è tecnica più sensibile della mammografia 2D perché ottimizza i vari aspetti menzionati. L’impianto mammografico viene modificato per consentire alla sorgente radiogena di ruotare ed eseguire radiografie del seno a diversi angoli di proiezione; le immagini digitali, acquisite a bassa dose, sono poi opportunamente combinate per ricostruire le sezioni a diversa profondità. La tomosintesi in pratica è una mammografia migliore. Nata per superare i limiti della mammografia digitale 2D la tomosintesi permette di ricostruire una stratigrafia della mammella a partire da un numero finito di proiezioni bidimensionali. Di ultimissimo sviluppo è il CAD che mediante marker segnala le aree di maggiore interesse.
- Digital breast tomosynthesis (DBT): è una tomografia ad angolo limitato applicata alla mammografia
- E’ tecnologia di recente introduzione e di forte impatto per la detezione e la diagnosi della patologia mammaria.
- Permette di ricostruire a strati secondo piani paralleli al detector 2 D, con un effetto “pseudo 3D”.
Ciò contribuisce a ridurre gli artefatti da sovrapposizione o sommazione e ad ovviare al mascheramento delle lesioni relativo alla densità mammaria. La tomosintesi è in grado di visualizzare separatamente oggetti posti a profondità diverse tramite l’acquisizione di molteplici proiezioni bidimensionali a bassa dose per diverse angolazioni del tubo rx intorno alla mammella con detettore fermo. I dati acquisiti vengono ricostruiti in una serie di strati sottili ad alta risoluzione.
Le finalità
- Individuare lesioni che ora sfuggono alla mammografia digitale riducendo i cancri d’intervallo
- Ridurre il numero dei falsi positivi
- Incidere sul tasso di richiami nei programmi di screening
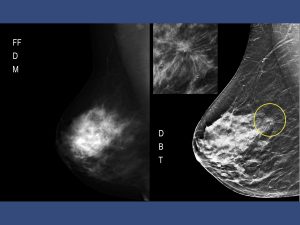
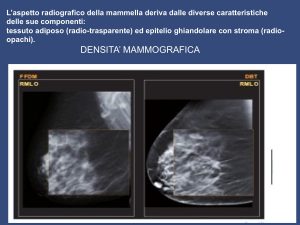
- Limiti della mammografia
● mammelle opache, ghiandolari,
● sede marginale del tumore,
● scarsa densità (opacità) intrinseca del tumore,
● tumore molto piccolo,
● contorni regolari di alcuni tumori,
● difetti di apparecchiature e di esecuzione dell’esame.
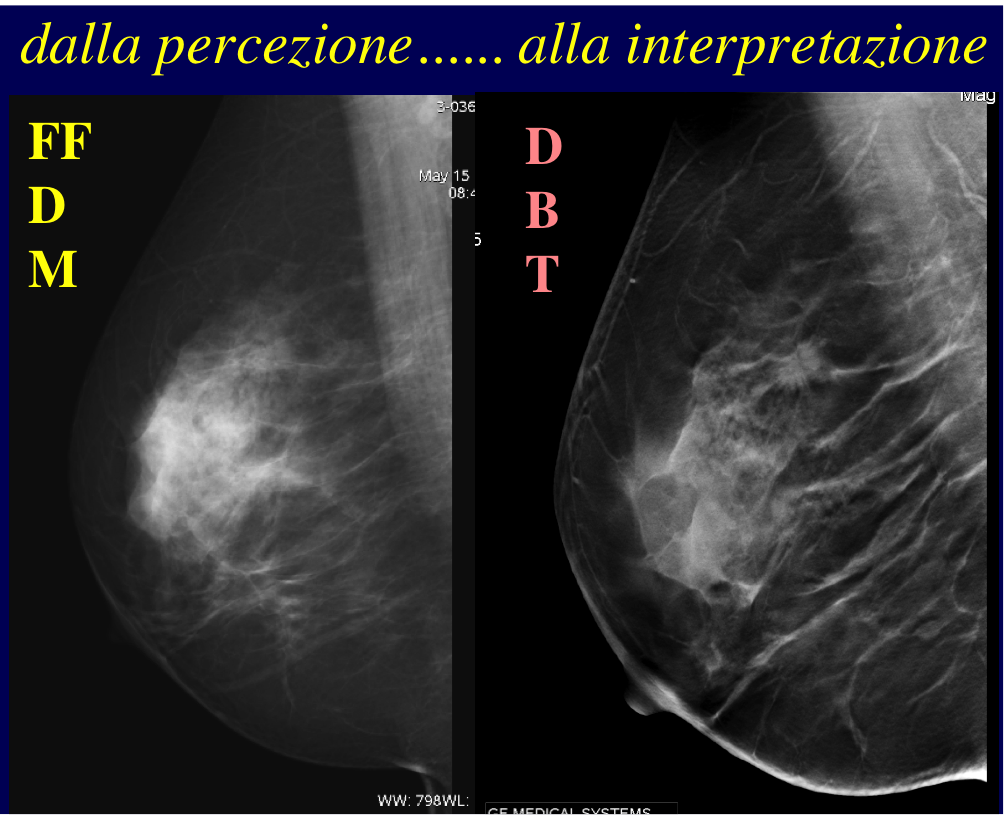
- La tomosintesi è in grado di visualizzare separatamente oggetti posti a profondità diverse tramite l’acquisizione di proiezioni a bassa dose per diverse angolazioni del tubo rx intorno alla mammella con detettore fermo. Idati acquisiti vengono ricostruiti in una serie di strati sottili ad alta risoluzione. A differenza della Mammografia, in cui i tessuti appartenenti a piani dello spazio diversi risultano sovrapposti nella immagine mammografica, nella Tomosintesi è possibile esaminare la mammella a strati di piccolo spessore, e quindi avere una precisa immagine di ogni strato, riducendo le “false” immagini dovute alla sovrapposizione delle strutture, tipica della Mammografia.
Fino a poco tempo fa l’esecuzione della Mammografia 3D comportava un’esposizione aggiuntiva ai raggi X, rispetto alla Mammografia 2D. Oggi invece grazie al software C-View, permette di eseguire Mammografia 2D e Tomosintesi con la stessa dose della Mammografia “low dose”, quindi con minima esposizione della paziente ai raggi X. Le immagini della Tomosintesi sono esaminate assieme alle immagini 2D, essenziali per la valutazione della mammella nel suo insieme, il confronto con gli esami precedenti e il rapido riconoscimento delle microcalcificazioni
La ricostruzione 3D supera i limiti della Mammografia 2D dovuti a densità mammaria e sovrapposizione dei tessuti che determinano mascheramento e misconoscimento dei tumori.
La differenza più importante con la mammografia è l’uso di una sorgente a raggi X in movimento in tomosintesi. Durante un esame di tomosintesi, la sorgente a raggi x si muove dopo un arco sopra il seno e acquista diverse proiezioni. Alla fine, vengono ottenute numerose immagini, ognuna delle quali mostrando uno strato del seno [ 19 , 20 , 21]. La tomosintesi può essere acquisita come un’immagine aggiuntiva ai mammografi usuali o può essere acquisita da sola. Quest’ultimo protocollo è possibile perché le immagini molto simili ai mammografie usuali possono essere ricostruite dal set dei dati di tomosintesi: questi cosiddetti mammografi sintetici possono evitare la necessità di acquisire i mammografie originali originali [ 20 , 22 ]. Secondo il dispositivo utilizzato, l’esposizione alle radiazioni è uguale a leggermente superiore rispetto alla mammografia, ma è ancora nei limiti raccomandati dalle linee guida internazionali sulla sicurezza delle radiazioni [ 23]. I risultati di diversi studi che confrontano solo la mammografia con la mammografia con tomosintesi hanno dimostrato che la tomosintesi è in grado di aumentare significativamente il rilevamento del cancro fino al 30-40% [ 21 ].
La tomosintesi è già usata come modalità di screening negli Stati Uniti. In Europa, solo alcuni centri eseguono la tomosintesi nei programmi di screening organizzati, soprattutto nel contesto di programmi di ricerca approvati dai comitati etici. I risultati di questi studi sono promettenti. Tre studi prospettici hanno dimostrato che DBT utilizzato come test aggiuntivo [ 24 , 25 , 26 ] o alternativa [ 27 ] ai comuni mammografi digitali consente una prestazione diagnostica superiore rispetto alla mammografia da solo. Nel complesso, la tomosintesi fornisce un aumento del tasso di rilevazione da 0,5 a 2,7 per 1000 donne schermate, nonché una riduzione del tasso di richiamo da 0,8 a 3,6 per 100 donne schermate [ 28]. Tutti questi aspetti conferiranno probabilmente alla tomosintesi lo status di futura mammografia di routine anche nell’ambito dello screening.
Tuttavia, prima di introdurre la tomosintesi nella screening del cancro al seno al di fuori di prove eticamente omologate, ci dovrebbe essere prova di una riduzione statisticamente significativa e clinicamente rilevante del tasso di tumore dell’intervallo. Questa cautela è dovuta alla necessità di evitare un aumento dei costi. I primi risultati di una riduzione da 0,7 a 0,5 intervalli di cancro per 100 donne scrinate sono stati recentemente riportati da un grande studio negli Stati Uniti [ 29 ], ma ulteriori prove sono necessarie.
Durante l’esame del seno eseguito al di fuori dell’ambiente di screening, è la scelta del radiologo di eseguire solo mammografia, di associare tomosintesi e / o ultrasuoni, oppure di eseguire la tomosintesi senza mammografia standard e di ottenere mammografia sintetica ricostruita. Questa decisione si basa su vari aspetti: le caratteristiche del seno, la disponibilità di esami precedenti, la disponibilità della tecnologia e anche la preferenza del radiologo in relazione al caso specifico.
Per le donne: Nota I. Se siete invitati a partecipare a un programma di screening in cui la tomosintesi è proposta nel contesto di uno studio o come pratica di routine, considerate che i potenziali vantaggi della tomosintesi in termini di aumentato rilevamento del cancro e ridotto tasso di richiamo dovrebbero superare il trascurabile aumento dose di radiazioni.
Gli studi clinici pubblicati hanno dimostrato che la tomosintesi ha dimostrato un incremento in sensibilità e in specificità’ con una riduzione dei falsi positivi compresa tra il 17 e il 37%, consentendo di riconoscere neoplasie non visibili con la mammografia bidimensionale, dal 27 al 40% in più a seconda degli studi e di meglio definire le eventuali alterazioni presenti.
I VANTAGGI DELLA MAMMOGRAFIA DIGITALE 3D CON TOMOSINTESI
- Analisi più accurata eliminando gli artefatti da sovrapposizione del tessuto fibroghiandolare, incrementando la risoluzione spaziale e riducendo i falsi negativi e i falsi positivi. I falsi negativi della mammografia digitale oscillano dal 10 al 30%.2. La dose di radiazione ampiamente al di sotto della dose di sicurezza, sostanzialmente analoga alla mammografia digitale ma di gran lunga inferiore rispetto alla mammografia analogica.3. La Tomosintesi c-view permette l’esecuzione della mammografia in 3D con ricostruzione mediante algoritmo matematico di una immagine 2D.
Vantaggi:
- riduzione numero richiami
- maggior valore predittivo positivo
- minor numero di falsi positivi e falsi negativi
- riduzione dei cancri intervallo
- miglior indice di concordanza diagnostica
In tomosintesi i particolari anatomici realmente presenti nel piano esaminato, appaiono perfettamente “a fuoco” e quindi con una evidenza (rapporto segnale/rumore) molto maggiore.
La ricostruzione a strati della tomosintesi riduce o elimina i problemi causati dalla sovrapposizione dei tessuti, anche se il limitato angolo di rotazione (rispetto alla rotazione di 360° della TC) non consente una completa cancellazione dei particolari contenuti nei piani sovra o sottostanti rispetto a quello di interesse (“ombre di trascinamento”).
Uno studio recente ha analizzato i risultati di 12.631 esami interpretati utilizzando la sola mammografia e la mammografia più la tomosintesi. I ricercatori hanno scoperto che con la mammografia più la tomosintesi c’era un aumento del 31% nel tasso di identificazione del cancro; il tasso di falsi positivi era del 13% in meno; e c’è stato un aumento del 26% nel rilevamento di tumori di grado elevato. 6
In un altro studio, condotto da Liane Philpotts, MD, Chief of Breast Imaging presso la Yale University School of Medicine di New Haven, CT, gli investigatori hanno concluso che l’aggiunta di 3D a un esame di screening ha ridotto i tassi di richiamo del 40%. 7
Mammogrammi più esami ausiliari
Secondo l’American College of Radiology Imaging Network (ACRIN), circa il 40% di tutte le donne sottoposte a mammografia di screening hanno seni densi. 4 “C’è il problema del mascheramento del cancro del seno a causa della densità del seno. Tutti concordano poi sul fatto che esiste un maggior rischio di cancro al seno nelle donne con seno denso “, ha affermato Dennis McDonald, direttore medico per l’imaging del seno presso il Sutter Medical Center Sacramento, Sacramento, CA.
Per risolvere il problema, il centro ha implementato il software Volpara per la misurazione della densità del seno, uno strumento di valutazione della densità del seno per migliorare la diagnosi precoce tra nelle donne con seno denso. Volpara genera automaticamente misurazioni oggettive e automatiche dei valori volumetrici della densità del seno con Volpara Density Grade (VDG ® ), un sistema di classificazione correlato con le classificazioni della densità BI-RADS dell’American College of Radiology. Volpara è stato approvato dalla FDA per tutte le unità di mammografia digitale e sono in corso anche l’integrazione con altri sistemi di mammografia digitale, sistemi CAD e soluzioni di segnalazione mammografica.
“Abbiamo acquistato il software Volpara per dare una stima più obiettiva della densità del seno perché è una misurazione volumetrica. Nella nostra esperienza, c’è davvero una buona correlazione con la nostra interpretazione visiva; ha dato una certa coerenza all’intero processo di determinazione della densità “, ha affermato il dott. McDonald.