Lo screening mammografico riduce la mortalità per cancro al seno in pazienti di età compresa tra 40 e 80 anni.
Poiché la mortalità aumenta con l'età, lo screening all'età di 70 anni è più vantaggioso dello screening all'età di 48 anni.
Recenti studi raccomandano di eseguire dieci screening mammografici ogni due anni a partire dall'età di 50 anni.
Se un programma di screening mammografico dovesse essere ampliato, il beneficio deve essere dimostrato per ogni età aggiuntiva.
È stato dimostrato che lo screening con mammografie aumenta il tasso di sopravvivenza a 20 anni dal 68% (pazienti non sottoposti a screening) all'83% (pazienti sottoposti a screening).
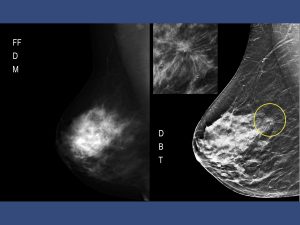
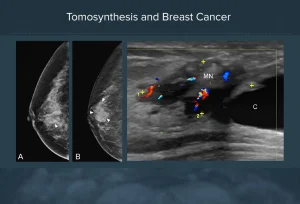
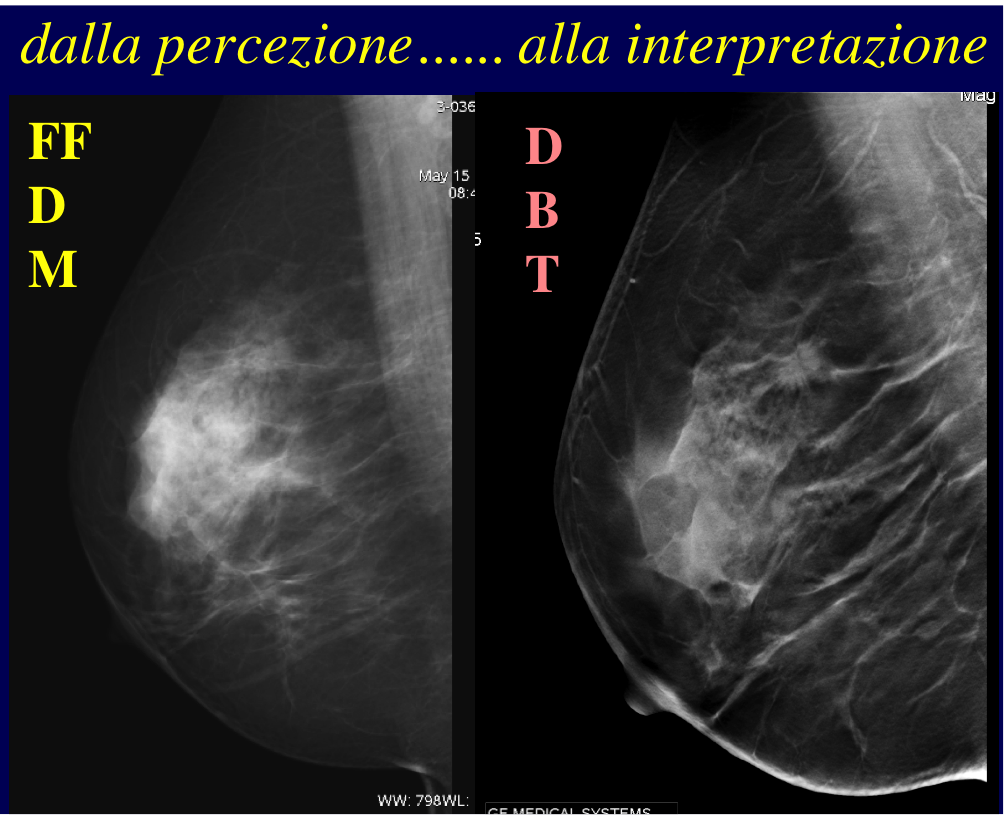
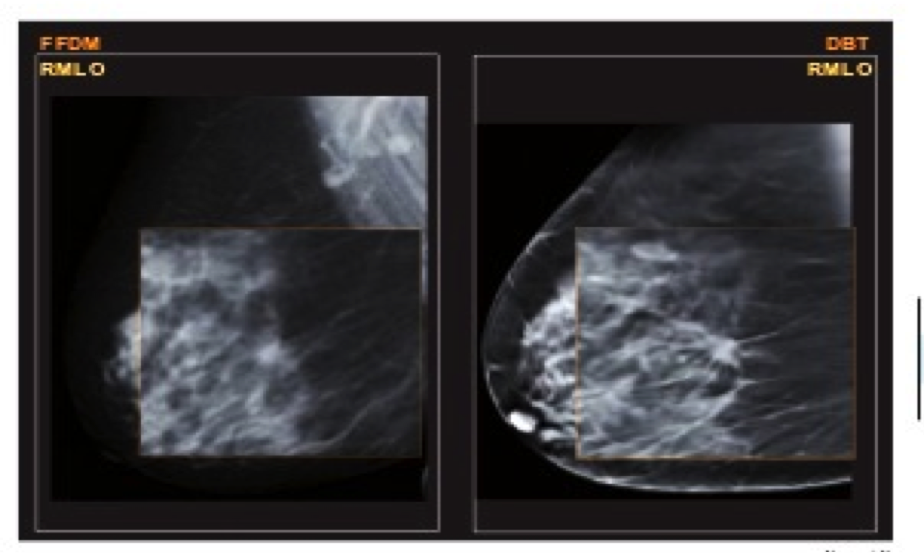
La ricostruzione 3D supera i limiti della Mammografia 2D dovuti alla densità mammaria ed alla sovrapposizione dei tessuti che determinano mascheramento e misconoscimento dei tumori.
Vantaggi della tomosintesi mammaria digitale rispetto alla mammografia digitale diretta:
– maggior detection rate dei carcinomi invasivi, ma anche non invasivi – riduzione numero richiami – maggior valore predittivo positivo – minor numero di falsi positivi e falsi negativi – riduzione dei cancri intervallo – miglior indice di concordanza diagnostica intra e inter-lettore.
Febbre di Tomosintesi
Dieci anni fa cosa diceva Stefano Ciatto, eravamo all’inizio…
“Più lavoro con la tomosintesi (chiamiamola 3D che si risparmia, visti i tempi) e più mi entusiasmo, il che è per lo meno inquietante conoscendo quanto io sia scettico, critico e distruttore. Ma verificare con una discreta frequenza quanto la 3D possa evidenziare un cancro, anche non piccolo, del tutto occulto alla 2D è assolutamente entusiasmante, per tacere di quanti dubbi per addensamenti “costruiti” riesca a risolvere.
La ricerca nel campo sta imperversando, per fortuna, e anche in Italia ci si da da fare in varie sedi. Alcuni aspetti della metodica sono chiari:
– l’impegno per un TSRM è poco superiore. Ottenere immagini 2D+3D comporta un 10% di tempo in più rispetto alle 3D (almeno con Hologic che ha bassi tempi di scansione)
– l’impegno della lettura per il radiologo praticamente raddoppia, per leggere 2D+3D, rispetto alla 2D. Questo è un limite rispetto ad un possibile uso di screening
– la dose è circa doppia (con 2D+3D rispetto a 2D): nell’età di screening (50-69) non è un problema visto il rischio di cancerogenesi trascurabile, ma resta sempre un problema con cui confrontarsi nelle donne più giovani
– la 3D abbatte i richiami, risolvendo le immagini da sommazione: parliamo da un 40 a un 70% nei vari studi finora condotti !
Ma ci sono tanti punti da chiarire:
– quanto (se) aumenta la sensibilità: siamo ormai pieni di casi aneddotici di cancri non visti in 2D e evidenti in 3D: i corsi itineranti lo stanno dimostrando in tutta Italia. Quello che manca è una misura precisa del tasso diagnostico incrementale. Uno studio di screening è in corso a Trento e Verona e si spera che altri si aggiungano. E’ possibile che per Giugno si abbiano risultati interessanti
– quanto (se) diminuisce il tasso di richiamo in screening. L’abbattimento dei richiami per ora è stato testato su casistiche selezionate e non in pratica corrente di screening. Gli studi sopra indicati risponderanno anche a questo quesito e in minor tempo che per la detection rate di cancro
– se è competitivo con la RM per la stadiazione (sempre che sia utile stadiare con RM…). Torino e Trento stanno raccogliendo casistica e si spera che possano presentare uno studio cumulativo a breve
– i costi. Dovranno essere confrontati con i benefici, ancora ignoti, ma saranno un probema, anche se è probabile che con la diffusione della metodica i costi si possano abbattere
– nuovi sviluppi tecnologici: la possibilità di creare una immagine 2D “sintetizzata” a partire dalle acquisizione della 3D è già una realtà. Se dovesse anche solo equivalere alla 2D convenzionale avremmo risolto il fastidioso problema della dose. Lavori in corso
– possibile impiego in alternativa alla doppia lettura: il confronto tra doppia lettura 2D e lettura singola 2D+3D è in atto, almeno nello studio di screening di TN e VR.
Se la risposta fosse positiva avremmo risolto anche il problema dei tempi di lettura, che resterebbero doppi ma dimezzando i radiologi, quindi conto pari… Come vedete c’è tanta carne al fuoco.
Seguite l’argomento, che è la bomba del decennio e merita. POSTED ON 6 dicembre 2011
Tutte le donne e i medici che hanno conosciuto Stefano Ciatto hanno potuto apprezzare il suo rigore scientifico ed il suo spirito critico. Molti medici hanno imparato da lui, molti hanno sviluppato la cultura dello screening e della diagnosi precoce. Tutti abbiamo apprezzato la sua onestà intellettuale e la sua rigorosa metodologia scientifica. Stefano Ciatto accolse con entusiasmo la tomosintesi e invitava tutti a continuare in ricerca e innovazione con rigore scientifico.
Premessa
Limiti della mammografia
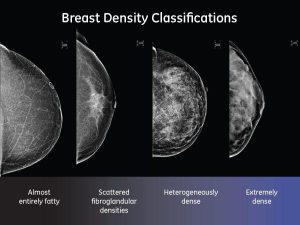
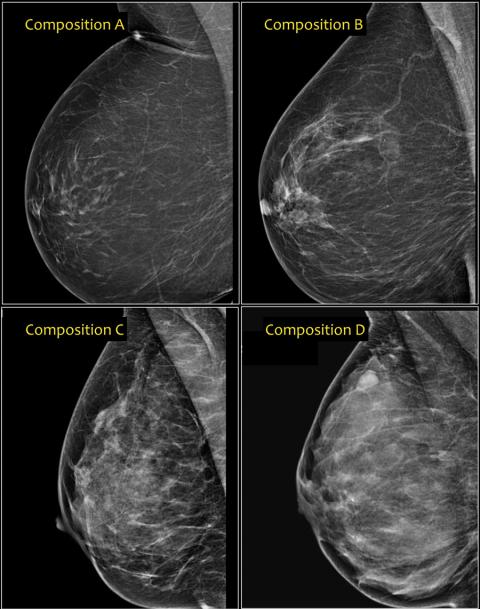
● mammelle opache, ghiandolari (densità c e d),
● sede marginale del tumore,
● scarsa densità (opacità) intrinseca del tumore,
● tumore molto piccolo,
● contorni regolari di alcuni tumori,
● difetti di apparecchiature e di esecuzione dell’esame.
E’ indubbio che il modo più naturale ed efficace per rimuovere il cosiddetto rumore strutturale in mammografia consista nel separare fisicamente le varie strutture anatomiche del seno. La mammografia rappresenta infatti una proiezione bidimensionale di una struttura tridimensionale per cui, geometricamente, tessuti appartenenti a piani diversi risultano sovrapposti nell’immagine radiografica. Non c’è nulla di nuovo in tutto ciò, semplicemente la tecnologia tomografica ha raggiunto la maturità anche per la diagnosi precoce del tumore al seno per cui sistemi dedicati sono in fase di applicazione clinica.
La Tomografia è una tecnica ben nota in radiologia che utilizza il movimento per meglio esibire l’anatomia in modo pertinente, consentendo, nel contempo, a strutture sovrapposte di svanire. L’esempio più pervasivo è oggi la tomografia computerizzata (CT). Più recentemente, questo stesso concetto è stato applicato nella formazione dell’immagine del seno con lo sviluppo della tomosintesi. Interesse avviato nel 1990 quando divennero disponibili rivelatori a pannello piatto. [1] Nel 2011, Hologic, Inc (Bedford, MA) ha ricevuto l’approvazione FDA per il sistema 3D Selenia, un sistema tridimensionale (3D) che era l’unico sistema di tomosintesi del seno approvato dalla FDA .
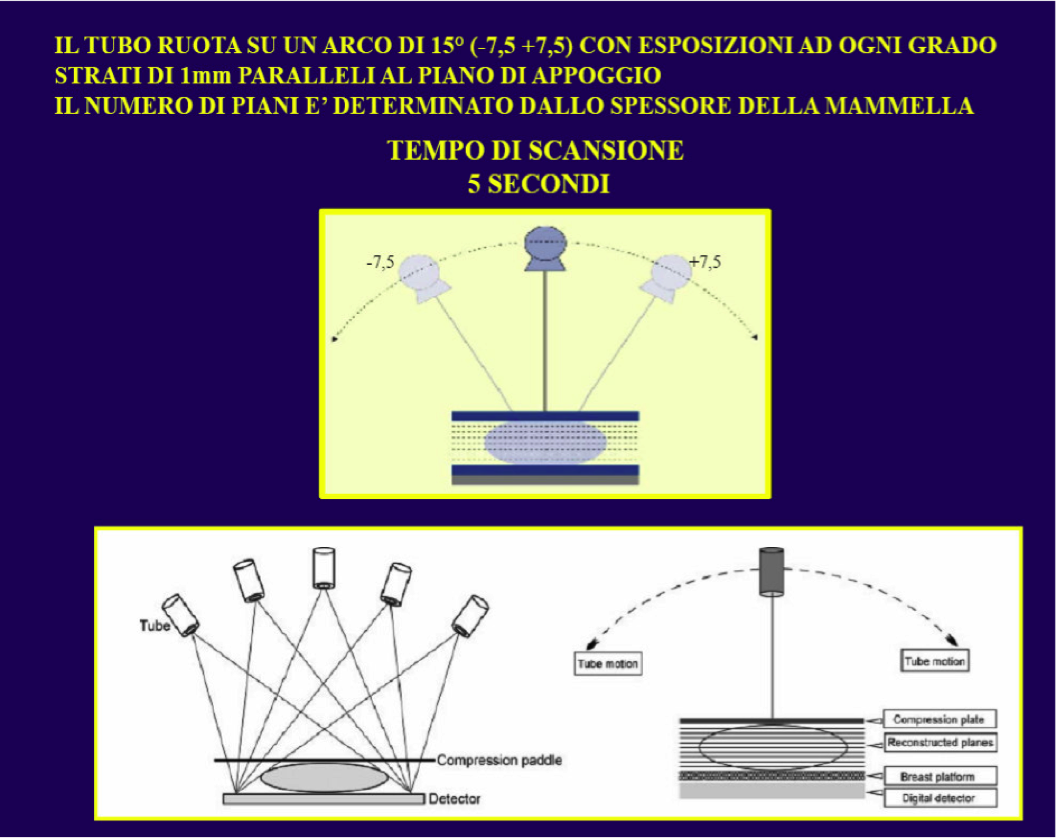
ll tubo a raggi X compie un arco di rotazione (da ± 8 a ± 30 a seconda dei sistemi) rispetto all’asse verticale raccogliendo una serie di “proiezioni” della mammella sotto diversi angoli, mentre rimangono fermi la mammella ed il detettore. Le immagini vengono rielaborate con algoritmo analogo a quello a quello impiegato in TC. La mammella è visualizzata scorrendo le immagini corrispondenti a diverse sezioni d’organo perpendicolari all’asse verticale. Oggi invece grazie al software C-View, permette di eseguire Mammografia 2D e Tomosintesi con la stessa dose della Mammografia “low dose”, quindi con minima esposizione della paziente ai raggi X. Le immagini della Tomosintesi sono esaminate assieme alle immagini 2D, essenziali per la valutazione della mammella nel suo insieme, il confronto con gli esami precedenti e il rapido riconoscimento delle microcalcificazioni
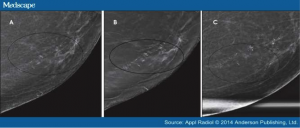
La Tomosintesi acquisisce immagini (~ 15 immagini) utilizzando un angolo stretto di movimento. Nelle screening, sia la craniocaudale(CC) che la mediolaterale obliqua (MLO) sono acquisite.Tuttavia, le proiezioni supplementari possono essere ottenute se necessarie e giustificate. La sorgente di raggi x si muove in un unico piano in un arco intorno al seno..Queste immagini vengono poi ricostruite in immagini di spessore di 1 mm per la revisionee. La proiezione posteriore filtrata (FBP) è il metodo più comunemente usato per la ricostruzione, che è spesso usato per la ricostruzione di CT. [2]
Alcuni autori ponevano le seguenti domande: 1) Chi potrà beneficiare del 3D? 2) Come dovrebbe essere addebitato il 3D? 3) E’ il 3D valido sia per lo screening sia per la diagnosi ?4) Qual’è l’ impatto del 3D sul flusso di lavoro ? 5) Come influisce il 3d sul tempo di interpretazione ? 6) Come dovrebbero essere offerta la tomosintesi del seno? Il 3D dovrebbe essere offerto a tutte le donne o solo a quelle con seno denso?Dovrebbero le pazienti con noduli o pazienti sintomatiche effettuare il 3D? Inoltre, poiché la tomosintesi non è ancora rimborsata dalle compagnie di assicurazione sanitaria e non è ancora prevista l’entità del ticket il costo sarà assorbito dalla pratica o dovrebbe alla paziente essere addebitata una sovrattassa per compensando gli ulteriori costi di lavoro e costi di capitale?
L’integrazione della nuova tecnologia nella pratica clinica alterava dinamica e flusso del lavoro di una prassi consolidata. Per il radiologo e il tecnico sanitario, c’è stata una curva di apprendimento per una nuova modalità. Requisiti supplementari sono stati stabiliti anche per tecnici e fisici sanitari. Come osservato in precedenza, la tomosintesi , in media, raddoppia il tempo di interpretazione dello studio in rapporto all’ esame FFDM standard. La diffusione e popolarità della tomosintesi stanno producendo lunghe attese per molte donne. Tutti questi fattori richiedono la necessità di esaminare la donna personalmente negli ambulatori di senologia valutando requisiti e procedure di programmazione.
Negli Stati Uniti la Tomosintesi è proposta a tutte le donne che partecipano allo screening. Vi è stata una campagna promozionale rivolta alle donne e ai medici di riferimento, e le donne sono state molto ricettive alla nuova tecnologia. Per quanto riguarda la questione del rimborso, hanno una integrazione nominale al momento del servizio se la donna nello screening sceglie la tomosintesi. L’integrazione è stata considerata con attenzione nello stabilire tale importo. In ambito diagnostico, il paziente non ottiene la possibilità di scegliere o meno di sottoporsi ad un esame 3D. Piuttosto, la decisione è lasciata al radiologo nel momento in cui la donna si presenta. Il radiologo decide se mammografia 2D standard o tomosintesi debba essere utilizzata.
- Digital breast tomosynthesis (DBT): è una tomografia ad angolo limitato applicata alla mammografia
- E’ tecnologia di recente introduzione e di forte impatto per la detezione e la diagnosi della patologia mammaria.
- Permette di ricostruire a strati secondo piani paralleli al detector 2 D,
Ciò contribuisce a ridurre gli artefatti da sovrapposizione o sommazione e ad ovviare al mascheramento delle lesioni relativo alla densità mammaria. La tomosintesi è in grado di visualizzare separatamente oggetti posti a profondità diverse tramite l’acquisizione di 10- 20 proiezioni bidimensionali a basse dosi con diverse angolazioni del tubo rx intorno alla mammella con detettore fermo. I dati acquisiti vengono ricostruiti in una serie di strati sottili ad alta risoluzione.
Le finalità
- Individuare lesioni che ora sfuggono alla mammografia digitale
- Ridurre il numero dei falsi positivi
- Incidere sul tasso di richiami nei programmi di screening
Principio:
- Acquisire multiple proiezioni a bassa dose della mammella mediante un movimento angolare del tubo radiogeno e, successivamente, mediante software dedicati determinare una ricostruzione pseudo-tridimensionale della mammella.
Scopo:
- Aumentare la Sensibilità riducendo tutti gli effetti di sovrapposizione che possono comportare un mascheramento/misconoscimento delle lesioni evolutive della mammella;
- Aumentare la Specificità riducendo i dubbi/sospetti che questi fenomeni di sovrapposizione talora determinano.
La tomosintesi con Ciatto, già nel 2013 aveva dimostrato un incremento in sensibilità con un aumento della DR tra 0.5‰ e 2.7‰ e un incremento in specificità’ con una riduzione dei falsi positivi compresa tra il 17 e il 37% .
Aumento della sensibilità: Trento/Verona (STORM): 2.7 ‰
1) Ciatto S et al.: Lancet Oncol, 2013. 2) Skaane P et al.: Eur Radiol, 2013. 3) Rose SL et al.: Am J Roentgenol, AJR 2013. 4) Haas BM et al.: Radiology, 2013. 5) Interim analysis: presented at the ECR, Vienna, 2013
La Tomosintesi oggi nella pratica clinica
La mammografia 3D migliora l’identificazione di tumori nelle mammelle dense
- Phi XA & al.
- Nelle donne con mammelle dense, la mammografia digitale con tomosintesi (digital breast tomosynthesis, DBT, nota anche come mammografia 3D) ± mammografia digitale (digital mammography, DM) è migliore della sola DM per l’identificazione del carcinoma mammario in ambito sia diagnostico sia di screening.
- La DBT può essere anche migliore nel ridurre il tasso di ulteriori accertamenti.
Perché è importante
- I risultati favoriscono l’uso di DBT±DM rispetto a sola DM nelle donne con mammelle dense.
Disegno dello studio
- Metanalisi di 16 studi (n=5 studi diagnostici; n=11 studi di screening) che soddisfacevano i criteri di eleggibilità dopo una ricerca su PubMed e Web of Science.
Risultati principali
- Negli studi diagnostici la DBT ha evidenziato una sensibilità maggiore (84%–89%) rispetto alla DM (69%–86%), ma la specificità era simile.
- Negli studi diagnostici DBT±DM hanno aumentato il tasso di identificazione di tumori (cancer detection rate, CDR) rispetto alla DM (rapporto di rischio [RR]: 1,12; IC 95%: 1,01–1,24).
- Negli studi di screening DBT±DM hanno aumentato il CDR rispetto alla DM (RR: 1,33 [IC 95%: 1,20–1.47] per gli studi retrospettivi e 1,52 [IC 95%: 1,08–2,11] per gli studi prospettici).
- Negli studi di screening il tasso di ulteriori accertamenti era inferiore con DBT±DM rispetto a sola DM negli studi retrospettivi (RR: 0,72; IC 95%: 0,64–0,80), ma non negli studi prospettici (RR: 1,12; IC 95%: 0,76–1,63).
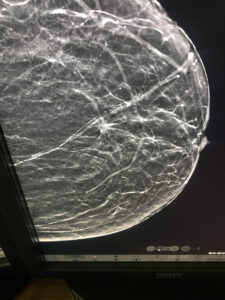
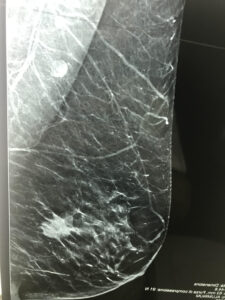
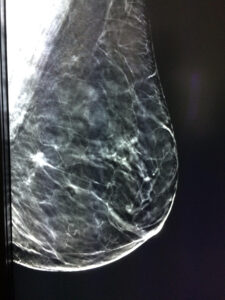
Vantaggi della tomosintesi mammaria digitale:
-maggior detection rate dei carcinomi invasivi, ma anche non invasivi
-riduzione numero richiami
-maggior valore predittivo positivo
-minor numero di falsi positivi e falsi negativi
-riduzione dei cancri intervallo
-miglior indice di concordanza diagnostica
In tomosintesi i particolari anatomici realmente presenti nel piano esaminato, appaiono perfettamente “a fuoco” e quindi con una evidenza (rapporto segnale/rumore) molto maggiore. La ricostruzione a strati della tomosintesi riduce o elimina i problemi causati dalla sovrapposizione dei tessuti, anche se il limitato angolo di rotazione (rispetto alla rotazione di 360° della TC) non consente una completa cancellazione dei particolari contenuti nei piani sovra o sottostanti rispetto a quello di interesse (“ombre di trascinamento”).
Ad oggi, il ruolo della tomosintesi è stato stabilito per la popolazione di screening. C’è un aumento del tasso di rilevazione del cancro, diminuendo il tasso di richiamo.
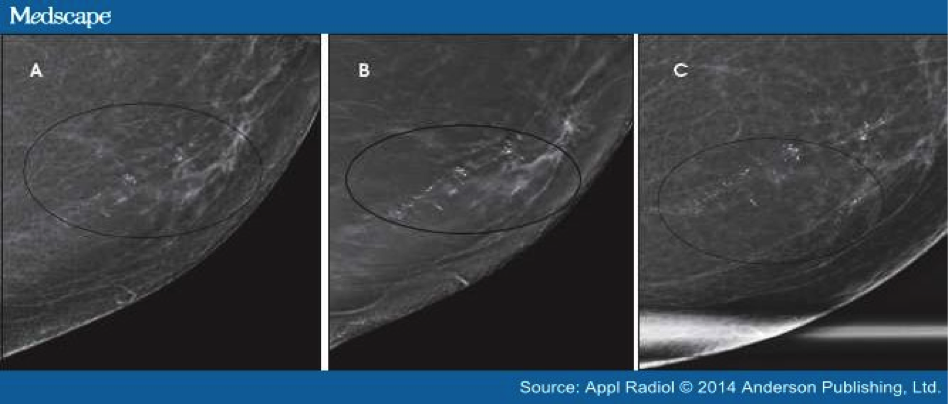
La morfologia delle microcalcificazioni è evidenziabile come in Mammografia 2D(vedi B)
Conclusioni: Tomosintesi “Una mammografia migliore”
La Mammografia 3D, o tomosintesi digitale del seno, è in grado di individuare i tumori significativamente più invasivi della mammografia digitale convenzionale, riducendo esami di follow-up non necessari, secondo una retrospettiva studio pubblicato nel numero del 25 Junea JAMA . Il tasso di individuazione dei carcinomi più invasivi è aumentato del 41% dopo. Il tasso dei carcinomi duttali in situ (DCIS) è rimasto la stesso. L ’uso di tomosintesi ha anche ridotto il numero di donne che sono state richiamate per proiezioni inutili a causa di falsi allarmi del 15%.
“E il più emozionante miglioramento che ho visto nella mia carriera, ancora più importante che la conversione da pellicola a schermo mammografia per mammografia digitale,” ha detto l’autore senior Emilya F. Conant, MD, capo delle immagini del seno in Dipartimento di Radiologia presso la Scuola Perelman di Medicina dell’Università della Pennsylvania, a Filadelfia, in un comunicato.
Come esame di diagnosi precoce la tomosintesi continuerà ad essere adottata in modo sempre più diffuso e speriamo capillare anche al Sud .
I VANTAGGI DELLA MAMMOGRAFIA DIGITALE 3D CON TOMOSINTESI
- Analisi più accurata eliminando gli artefatti da sovrapposizione del tessuto fibroghiandolare, incrementando la risoluzione spaziale, riducendo i falsi negativi e i falsi positivi. I falsi negativi della mammografia digitale oscillano dal 10 al 30%.
- La dose di radiazione ampiamente al di sotto della dose di sicurezza, sostanzialmente analoga alla mammografia digitale ma di gran lunga inferiore rispetto alla mammografia analogica.. L’apparecchiatura di cui siamo dotati (Tomosintesi c-view) permette l’esecuzione della mammografia in 3D con ricostruzione mediante algoritmo matematico di una immagine 2D.
 Confronto 2D Tomosintesi
Confronto 2D Tomosintesi
Tomosintesi del seno con mammografia 3D nello screening del tumore al seno: una valutazione della singola tecnologia.
Editors
Movik E , Dalsbø TK , Fagelund BC , Friberg EG , Håheim LL , Skår Å .
Oslo, Norvegia: Centro informazioni per i servizi sanitari presso l’Istituto norvegese di sanità pubblica (NIPH); Rapporto di settembre 2017 dell’Istituto norvegese di salute pubblica n. 2017-08.
In Norvegia, lo screening del tumore al seno viene offerto attraverso un programma finanziato con fondi pubblici a donne della fascia di età 50-69 su base biennale. L’incidenza del cancro al seno è relativamente più alta tra le donne in questa fascia di età rispetto a quella delle donne più giovani. Lo scopo del programma di screening è ridurre la mortalità correlata al cancro al seno rilevando i tumori in una fase precedente. La tecnologia di screening in uso corrente, nota come mammografia digitale (DM), consiste nel catturare due immagini bidimensionali di ciascun seno da diverse angolazioni. Uno dei limiti di questa tecnologia è che i tumori possono essere “mascherati” e difficili da rilevare, specialmente nei seni densi. La tomosintesi mammaria digitale (DBT) può, quando utilizzata in combinazione con DM, alleviare questo problema fornendo un modello 3D del seno costruito sulla base di una serie di immagini 2D. La tecnologia include anche un’opzione per costruire immagini 2D “sintetiche” (S2D) simili a una mammografia digitale standard. I sistemi combinati hanno il potenziale per aumentare i tassi di rilevamento riducendo al contempo la necessità che il richiamo del paziente confermi o escluda la presenza di un tumore. Tuttavia, ciò significa che potrebbero essere rilevati ulteriori tumori che non richiedono un trattamento durante la vita del paziente, aumentando così il tasso di sovradiagnosi. Lo screening mammografico comporta l’esposizione alle radiazioni, un fattore che deve essere preso in considerazione quando vengono valutate nuove tecnologie di screening. “Bestillerforum” ha richiesto al National Institute of Public Health di eseguire una valutazione di una singola tecnologia (STA) relativa alla “Tomosintesi tridimensionale del seno digitale nello screening per il cancro al seno” (ID2015_041) il 25 gennaio 2016.
Obiettivo L’obiettivo di questa valutazione della singola tecnologia (STA) è valutare l’efficacia, la sicurezza e l’efficacia in termini di costi della tomosintesi digitale del seno nello screening del carcinoma mammario in Norvegia. Esistono diversi produttori di sistemi DBT, ma solo Hologic Inc., ad oggi (giugno 2017) ha presentato un pacchetto di documentazione. Abbiamo eseguito una singola valutazione della tecnologia sull’uso del sistema di mammografia digitale Hologic Selenia Dimensions per lo screening del carcinoma mammario, basato sulla presentazione da parte di Hologic Inc. Non copriamo l’uso del sistema nella diagnosi di cancro al seno nella pratica clinica da parte di questo STA.
Valutazione della documentazione, Efficacia clinica La documentazione presentata dalla società consisteva in 12 studi identificati da una ricerca sistematica della letteratura. Quattro pubblicazioni hanno soddisfatto i nostri criteri di inclusione e sono incluse per la valutazione in questo STA. Abbiamo valutato la presente documentazione utilizzando un PICOS predefinito (Popolazione, Intervento, Comparatore, Risultati e progettazione dello studio), rischio di valutazione di bias dei dati forniti dal file di presentazione, estrazione dei dati e valutato la certezza delle prove per le stime utilizzando la valutazione GRADE (Grades of Recommendation, Assessment, Development and Evaluation). Abbiamo anche esaminato l’analisi costo-efficacia e l’analisi dell’impatto del budget descritte nella submission.
Dose di radiazioni e valutazione del rischio Il richiedente non ha fornito alcuna documentazione che valuti il rischio associato alla dose di radiazioni con DBT. Pertanto, abbiamo condotto una valutazione separata dei potenziali rischi associati all’esposizione alle radiazioni con DBT.
Risultati, Efficacia clinica I nostri risultati principali sono i seguenti: Non siamo sicuri se la tomosintesi digitale mammaria in combinazione con mammografia digitale o mammografia digitale sintetizzata diminuisca o aumenti i tassi di richiamo rispetto alla mammografia digitale da sola (fiducia molto bassa a causa di prove contrastanti da studi osservazionali). L’intervento può aumentare il tasso di tumore individuato dallo screening (tasso di rilevamento del cancro (CDR) in base a tutti gli studi (fiducia molto bassa dovuta a scarsa evidenza da uno studio osservazionale). Non siamo sicuri se la tomosintesi digitale mammaria in combinazione con mammografia digitale o La mammografia digitale synthezised fa la differenza per quanto riguarda la rilevazione del cancro a intervalli rispetto alla sola mammografia digitale (scarsa sicurezza nelle prove a causa di prove sparse provenienti da uno studio osservazionale). Non siamo sicuri se la tomosintesi digitale mammaria in combinazione con mammografia digitale o mammografia digitale sintezizzata diminuisca o aumenti i tassi di falsi positivi rispetto alla mammografia digitale da sola (fiducia molto bassa a causa di prove contrastanti da studi osservazionali). L’intervento può fornire tassi di sensibilità simili, ma può aumentare i tassi di specificità (bassa attendibilità a causa di evidenze provenienti da studi osservazionali). Non siamo sicuri se la tomosintesi digitale mammaria in combinazione con mammografia digitale o mammografia digitale sintetizzata diminuisca o aumenti i tassi di falsi negativi rispetto alla mammografia digitale da sola (fiducia molto bassa a causa della scarsa evidenza da uno studio osservazionale). Non sono state riportate informazioni sulla morte e sulla qualità della vita.
Dose di radiazioni e valutazione del rischio Rispetto alla pratica corrente con DM, l’introduzione del sistema DBT di Hologic Selenia Dimensions nel norvegese Breast Cancer Screening Program (NBCSP) comporterà un’aumentata dose di radiazioni seguita da un aumento del rischio di cancro indotto da radiazioni per tutti gli interventi valutati definiti dal PICO. Riepilogo dei risultati sulla base delle dosi riportate nello studio OTST e STORM-2: solo DBT: la dose e il rischio aumenteranno dal 23% al 38%, risultando in una dose totale assorbita dal tessuto granulare (AGD) di 3,7-3,9 mGy e un’incidenza stimata di carcinoma mammario indotto da radiazioni da 15 a 16 su 100.000 donne e mortalità di 1,2 su 100.000 donne. DBT + DM: la dose e il rischio aumenteranno di un fattore compreso tra 2,23 e 2,37, risultando in un AGD totale di 6,4-7. 0 mGy e un’incidenza stimata di carcinoma mammario indotto da radiazioni da 26 a 29 ogni 100.000 donne e mortalità da 2,1 a 2,3 ogni 100.000 donne. DBT + S2D: la dose e il rischio saranno aumentati dal 23% al 38%, ma ridotti del 42% t0 45% rispetto a DBT + DM, con conseguente stessa dose e rischio del solo DBT. I valori stimati per l’incidenza del carcinoma mammario e della mortalità da radiazioni devono essere interpretati con cautela in quanto vi è un elevato livello di incertezza associato a questi. Tuttavia, il rapporto tra le dosi e i rischi per i diversi interventi fornisce un valido contributo alla valutazione del rapporto rischio-beneficio da eseguire per il programma di screening. risultando nella stessa dose e rischio della sola DBT. I valori stimati per l’incidenza del carcinoma mammario e della mortalità da radiazioni devono essere interpretati con cautela in quanto vi è un elevato livello di incertezza associato a questi. I valori stimati per l’incidenza del carcinoma mammario e della mortalità da radiazioni devono essere interpretati con cautela in quanto vi è un elevato livello di incertezza associato a questi. Tuttavia, il rapporto tra le dosi e i rischi per i diversi interventi fornisce un valido contributo alla valutazione del rapporto rischio-beneficio da eseguire per il programma di screening.Efficacia dei costi I risultati del caso base dell’analisi economica presentata di DBT + DM (S2D) rispetto al solo DM erano 0,007 anni di vita aggiustati per la qualità guadagnati per donna sottoposta a screening. Il costo incrementale per QALY guadagnato era di circa 144.000 NOK. Questo risultato è stimato per una popolazione di donne con seno denso. Hologic ha basato l’analisi dell’impatto del budget su tre componenti: costi relativi dell’approvvigionamento delle attrezzature, costi di screening e costi di trattamento del cancro al seno. La stima del caso base è stata un aumento netto delle spese di 77,5 milioni di NOK nell’anno 5 dopo l’attuazione. Hologic ha incluso anche l’analisi di sensitività nell’analisi dell’impatto del budget per determinare l’effetto di variare il prezzo, che deve ancora essere determinato, delle attrezzature DBT, e di esaminare come i cambiamenti nelle ipotesi importanti influenzerebbero i risultati dell’analisi dell’impatto del budget.
Discussione efficacia clinica e sicurezza Rispetto alla sola mammografia digitale, l’uso della tomosintesi digitale mammaria Hologic in combinazione con mammografia digitale standard o mammografia digitale sintetizzata può aumentare il tasso di cancro rilevato nello screening (tasso di rilevamento del cancro o CDR) secondo tutti gli studi. Gli studi hanno fornito prove sul primo ciclo di screening utilizzando DM + DBT, che potrebbe in parte spiegare il sostanziale aumento del tasso di rilevamento del cancro, rispetto allo screening standard con DM da solo. Le stime dei tassi di rilevamento del cancro per lo screening DBT ripetuto delle stesse popolazioni sono necessarie per quantificare l’effetto del DBT aggiuntivo sia sul rilevamento del cancro sia su richiami di falsi positivi a ripetuti cicli di screening. Gli studi randomizzati che valutano l’impatto del DBT aggiuntivo sui tassi di cancro da intervallo come surrogato per il beneficio dello screening fornirebbero prove critiche per sostenere la futura politica e pratica di screening della popolazione. Gli RCT dovrebbero essere progettati per affrontare simultaneamente ulteriori lacune nelle evidenze, come il rapporto costo-efficacia incrementale di DBT e misure di rilevamento a screening ripetuto con DBT aggiuntivo. L’utilizzo di DBT e DM standard (doppia acquisizione) provoca un aumento della dose di radiazioni. I sistemi DBT con la possibilità di generare immagini 2D sintetiche sono altamente favorevoli rispetto al DBT in combinazione con la mammografia digitale a pieno campo, a causa della sua riduzione della dose e del rischio associato. Le informazioni sulle dosi di radiazioni dovrebbero essere incluse nelle future sperimentazioni cliniche. Gli RCT dovrebbero essere progettati per affrontare simultaneamente ulteriori lacune nelle evidenze, come il rapporto costo-efficacia incrementale di DBT e misure di rilevamento a screening ripetuto con DBT aggiuntivo. L’utilizzo di DBT e DM standard (doppia acquisizione) provoca un aumento della dose di radiazioni. I sistemi DBT con la possibilità di generare immagini 2D sintetiche sono altamente favorevoli rispetto al DBT in combinazione con la mammografia digitale a pieno campo, a causa della sua riduzione della dose e del rischio associato. Le informazioni sulle dosi di radiazioni dovrebbero essere incluse nelle future sperimentazioni cliniche. Gli RCT dovrebbero essere progettati per affrontare simultaneamente ulteriori lacune nelle evidenze, come il rapporto costo-efficacia incrementale di DBT e misure di rilevamento a screening ripetuto con DBT aggiuntivo. L’utilizzo di DBT e DM standard (doppia acquisizione) provoca un aumento della dose di radiazioni. I sistemi DBT con la possibilità di generare immagini 2D sintetiche sono altamente favorevoli rispetto al DBT in combinazione con la mammografia digitale a pieno campo, a causa della sua riduzione della dose e del rischio associato. Le informazioni sulle dosi di radiazioni dovrebbero essere incluse nelle future sperimentazioni cliniche. I sistemi DBT con la possibilità di generare immagini 2D sintetiche sono altamente favorevoli rispetto al DBT in combinazione con la mammografia digitale a pieno campo, a causa della sua riduzione della dose e del rischio associato. Le informazioni sulle dosi di radiazioni dovrebbero essere incluse nelle future sperimentazioni cliniche. I sistemi DBT con la possibilità di generare immagini 2D sintetiche sono altamente favorevoli rispetto al DBT in combinazione con la mammografia digitale a pieno campo, a causa della sua riduzione della dose e del rischio associato. Le informazioni sulle dosi di radiazioni dovrebbero essere incluse nelle future sperimentazioni cliniche.
Efficacia/costi I risultati dell’analisi economica hanno indicato che la DBT aggiuntiva rispetto alla pratica di screening corrente potrebbe portare a una diagnosi precoce del carcinoma mammario con un tasso di richiamo più basso, sebbene le riduzioni dei costi potenziali risultanti da quest’ultima non siano effettivamente modellate. I risultati suggeriscono quindi che DBT aggiuntivo potrebbe essere efficace in termini di costi se adottato dal programma norvegese di screening del cancro al seno. Tuttavia, ci sono una serie di problemi che contribuiscono all’incertezza riguardo ai risultati. In primo luogo, l’incertezza sopra descritta per quanto riguarda l’efficacia clinica, in particolare per quanto riguarda la sensibilità, oltre le ripetute visite di screening e tra diverse popolazioni ( ad es.rispetto alla densità del seno). In secondo luogo, non sappiamo fino a che punto il potenziale aumento nell’individuazione del carcinoma mammario possa comportare un aumento della sovradiagnosi e un trattamento non necessario. In terzo luogo, poiché non è stato possibile fornire un modello economico sanitario adeguato e coerente, è difficile accertare l’impatto di varie ipotesi nell’analisi e valutare l’incertezza totale in merito ai risultati economici della salute.
Conclusione Ci sono troppe prove da trarre per quanto riguarda gli effetti dell’uso della tomosintesi digitale mammaria in combinazione con mammografia digitale o mammografia digitale sintetizzata rispetto alla mammografia digitale da sola per i risultati valutati nel nostro rapporto (tassi di richiamo, tasso di rilevamento del cancro, tasso di cancro da intervallo , tasso di falsi positivi e falsi negativi, sensibilità, specificità, mortalità e qualità della vita). La preparazione di una valutazione completa della tecnologia sanitaria dovrebbe essere presa in considerazione quando sono disponibili prove sufficienti.
Prove che oggi ci sono…
Copyright © 2017 di The Norwegian Institute of Public Health (NIPH).
Vantaggi della tomosintesi mammaria digitale rispetto alla mammografia digitale diretta:
• maggior detection rate dei carcinomi invasivi, ma anche non invasivi
• riduzione numero richiami
• maggior valore predittivo positivo
• minor numero di falsi positivi e falsi negativi
• riduzione dei cancri intervallo
• miglior indice di concordanza diagnostica intra e inter-lettore.
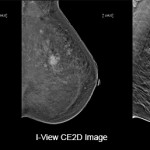
La nuova frontiera dell’imaging senologico: la mammografia 3D con mezzo di contrasto.
![]()
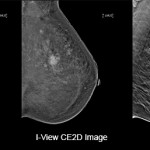
Mammografia con mezzo di contrasto (CEM)
Il tumore del seno è caratterizzato prevalentemente da un’area di nuova formazione di vasi (neoangiogenesi), pertanto la possibilità di evidenziare e studiare la presenza di queste aree è importante ai fini diagnostici”. Questo esame – molto veloce e ben tollerato dalle pazienti – permette di escludere completamente tutte le patologie benigne e di evidenziare solo le aree interessate dalla neoplasia. È un esame che dura 8 minuti ed è più accettabile della risonanza. della risonanza magnetica. La CEM è una nuova tecnica diagnostica che prevede l’iniezione venosa di mezzo di contrasto iodato e l’acquisizione in rapida sequenza di una coppia di immagini a bassa e ad alta energia. Dalla successiva “sottrazione” delle due immagini si ottiene una visualizzazione del contrasto. Il contrasto viene somministrato per via endovenosa e successivamente viene eseguita una mammografia a doppia energia. Si tentò inizialmente una strategia basata sulla sottrazione temporale (come in RM) di immagini ad alta energia la sottrazione temporale è stata abbandonata: compressione della mammella di lunga durata non confortevole per la paziente, artefatti da movimento, la compressione può ostacolare la normale perfusione del mezzo di contrasto.
In mammografia lo spettro X ha energie tipicamente con questa energia l’impregnazione di iodio ha un contrasto modesto. La CESM utilizza un fascio di energia superiore al k edge dello iodio (33 keV) per aumentare il contrasto la strategia è usare un fascio di alta energia fortemente filtrato per aumentare la componente di energia maggiore del k-edge dello iodio, aumentando il contrasto delle regioni impregnate di mdc e riducendo la dose alla paziente.
Trova applicazione nell’analisi vascolare dei noduli mammari sospetti scoperti con Ecografia e Mammografia: i noduli maligni, infatti, tendono a crescere e diventare più grandi in quanto alimentati dal flusso sanguigno. Viene inoltre indicata nelle pazienti con carcinoma accertato, in fase pre-chirurgica ai fini di stabilire se il focolaio è unico o multiplo, in chi è sottoposto a chemioterapia prima dell’intervento e nelle situazioni in cui la Risonanza Magnetica risulti non eseguibile.
L’utilizzo di mezzo di contrasto permette di evidenziare la proliferazione di vasi in prossimità del tumore (come in risonanza magnetica). Non a caso le masse tumorali sono in genere più ricche di vasi di un tessuto normale. Questo fenomeno è noto col nome di angiogenesi, cioè formazione di vasi.
Come per la risonanza, la base della mammografia spettrale a contrasto è il fatto che, durante lo sviluppo e la crescita un tumore forma e sviluppa nuovi vasi sanguigni per il nutrimento delle sue cellule. L’utilizzo del mezzo di contrasto permette di evidenziare i vasi sanguigni in prossimità del tumore. Per essere in grado di mostrare l’acquisizione del contrasto tumorale in un’immagine mammografica, è necessario acquisire due esposizioni del seno, ciascuna con una diversa composizione energetica dei raggi x, a basa ed alta energia, una possibilità tecnica disponibile per alcuni nuovi mammografi. Questo produce un’immagine a bassa energia come una mammografia normale, e un’immagine ad alta energia, dalla sottrazione delle due immagini si ottengono informazioni sulla distribuzione del contrasto nel seno; l’uso di energie diverse è la ragione della denominazione mammografia spettrale (CESM). A seconda della composizione e dello spessore del seno, questo provoca una dose di radiazioni supplementare di circa il 20%, ma entrambe le immagini insieme implicano una dose a raggi x al di sotto della dose raccomandata per la mammografia.
Mammografia con contrasto
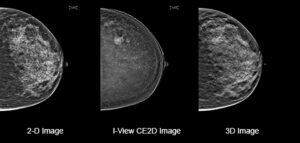
Una delle più potenti applicazioni tra le possibili modalità di imaging
-
- Lo screening di pazienti ad alto rischio (per esempio in caso di mutazione genetiche).
- Valutazione delle pazienti con sintomi/segni senologici (presenza di un nodulo palpabile, dolore costante solo ad un seno, secrezione dal capezzolo)
- Donne con densità mammaria marcata dove la mammografia normale mostra una sensibilità bassa.
- Donne claustrofobiche o che non possono eseguire un esame RMLa CEM unisce i principi della mammografia alla somministrazione del mezzo di contrasto (mdc) endovena, che permette, come in risonanza magnetica (RM), una valutazione contrastografica della mammella evidenziando le zone che captano il mdc, tipica espressione di neoangiogenesi neoplastica. La mammografia con mezzo di contrasto, detta anche CEM Contrast Enhanced Mammography, viene eseguita dopo l’iniezione di un liquido di contrasto iodato in vena.
Le principali indicazioni della mammografia con contrasto sono:
- Lo staging pre-operatorio (per determinare le dimensioni di una lesione tumorale nota o per studiare quei tumori che si presentano come lesioni multifocali o multicentriche).
- Lo studio prima di un trattamento chemioterapico.
- Lo studio dopo un trattamento chemioterapico per la valutazione di un eventuale residuo di malattia.
La mammografia con contrasto può essere usata infine per lo studio di lesioni dubbie come strumento “problem solving”.
Per l’esecuzione della mammografia con mezzo di contrasto è necessario che la paziente sia a digiuno e che abbia dosato la creatininemia per la valutazione della propria funzionalità renale. Inoltre, come tutti gli esami che usano radiazioni ionizzanti, non può essere eseguita in donne in gravidanza. I pazienti che hanno una storia di allergie, in particolare a farmaci, devono avere un colloquio con l’anestesista (presente durante l’esecuzione di un esame con mezzo di contrasto) per decidere una eventuale terapia antiallergica.
Quanto dura una mammografia con contrasto?
L’esame mammografico dura, dall’inizio dell’iniezione del mezzo di contrasto fino all’ultima immagine che viene ottenuta, 7-8 minuti massimo. La mammografia con mezzo di contrasto è un esame doloroso?
La mammografia con mezzo di contrasto è, tecnicamente parlando, identica a una mammografia standard, al quale si deve aggiungere l’eventuale fastidio soggettivo dell’iniezione del mezzo di contrasto per via endovenosa.
L’aggiunta di immagini di contrasto alla mammografia digitale 2D/3D standard migliora il rilevamento di neoplasie maligne ricorrenti o nuove in pazienti con una storia di tumore al seno
- Le donne con una storia di cancro al seno o carcinoma duttale in situ (DCIS) sono sottoposte a sorveglianza di routine per malattie nuove o ricorrenti.
- Gli ultrasuoni o la risonanza magnetica sono spesso usati per integrare la mammografia digitale.
- La mammografia con contrasto ha una sensibilità più elevata rispetto alla mammografia e agli ultrasuoni, nonché una migliore accessibilità rispetto alla risonanza magnetica.
- I risultati supportano l’uso della mammografia con contrasto per la sorveglianza di routine nelle sopravvissute al cancro al seno
La Mammografia con Mezzo di Contrasto (CEM) fornisce informazioni aggiuntive rispetto alla semplice mammografia che possono migliorare la capacità di rilevare lesioni. Con oltre 60 installazioni su territorio nazionale ed una letteratura sempre crescente, la mammografia con Mezzo di Contrasto Hologic (CEM) risulta ad oggi un esame totalmente affidabile, con una sensibilità paragonabile alla Risonanza Magnetica (MRI), ma con una specificità superiore 1, 2, 3. La Mammografia con Mezzo di Contrasto permette la visualizzazione di un farmaco, noto come mezzo di contrasto, la cui presenza é evidenziata nelle aree dove si sviluppano le lesioni erogando in rapida sequenza Raggi X a bassa e ad alta energia. I mezzi di contrasto usati sono gli stessi normalmente usati durante gli esami TAC.
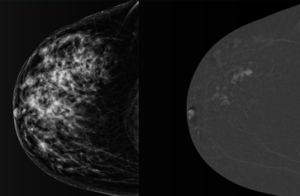
Grazie all’ultimo aggiornamento recentemente introdotto, si ottengono immagini funzionali ancora più nitide grazie a dedicati processing di riduzione degli artefatti da sottrazione ed attenuazione del BPE (Background Parenchymal Enhancement).
La Mammografia con Contrasto è caratterizzata da:
- Possibilità di procedure di reperaggio con metodica dual energy
- Co-registrazione con la mammografia 2D-3D con medesima compressione
- Velocità di esecuzione
- Semplicità della procedura
- Ridotta dose
- Qualità immagine aumentata, con riduzione del BPE ed artefatti
RIFERIMENTI
- A Petrillo, R Fusco, P Vallone, et al. Digital breast tomosynthesis and contrast‐enhanced dual‐energy digital mammography alone and in combination compared to 2D digital synthetized mammography and MR imaging in breast cancer detection and classification. The Breast, 2020 – Elsevier
- Bicchierai, P. Tonelli, A. Piacenti, et al. Evaluation of contrast‐enhanced digital mammography (CEDM) in the preoperative staging of breast cancer: Large‐scale single‐center experience. The Breast Journal, 2020 – Wiley Online Library
- Fallenberg EM, Schmitzberger FF, Amer H, et al. Contrast-enhanced spectral mammography vs. mammography and MRI – clinical performance in a multi-reader evaluation. European Radiology 2017 – Springer
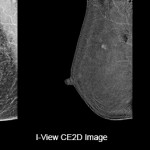
Sulla base di risultati ancora preliminari, la CESM può essere considerata come un’alternativa alla Risonanza con contrast-enhanced in caso vi siano controindicazioni alla Rm (inclusa la presenza di dispositivi non sicuri nel corpo del paziente, claustrofobia e obesità che impediscono al paziente di praticare la risonanza) o controindicazioni ad iniezione di contrasto a base di gadolinium o a causa di condizioni locali di difficoltà ad eseguire la risonanza.
Nota: è importante notare che gli agenti contrastanti iodati vengono spesso utilizzati nella pratica clinica, per lo più iniettati per via endovenosa per la tomografia. Ci sono controindicazioni (storia di reazioni allergiche, insufficienza renale) per i possibili effetti collaterali che richiedono discussione con il paziente e la firma di un consenso scritto. Quindi, l’iniezione di agenti di contrasto iodati per la mammografia richiede le stesse precauzioni utilizzate per altri esami basati sul contrasto. Prima dell’esame, il radiologo chiarirà i rischi e i benefici associati all’iniezione endovenosa di agenti contrastanti.
La strategia oggi utilizzata (CESM) prevede l’acquisizione in rapida sequenza di una coppia di immagini a bassa ed alta energia dalla “sottrazione” delle due immagini si ottiene una visualizzazione del contrasto
sviluppa vasi per il nutrimento delle cellule -> angiogenesi: processo fondamentale per la crescita della patologia da Pandya et al., Vascular Pharmacology, la CESM utilizza un fascio di energia superiore al k-edge dello iodio (33 keV) per aumentare il contrasto spettro simulato a 40 kVp anodo in rodio la componente dello spettro al di sotto del k-edge dello iodio non è utile per la formazione dell’immagine e fornisce solo una dose indesiderata
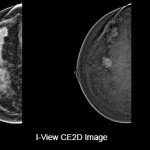
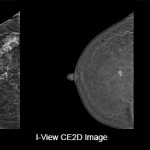
Per ogni cento carcinomi diagnosticati c’è la possibilità di identificarne ulteriori 13;
6 /100 lesioni benigne in più possono essere riconosciute correttamente;
19/100 pazienti in più cui non è stato diagnosticato il cancro possono essere congedate.
RM
Tecnica volumetrica;
Risoluzione di contrasto;
Onde radio;
Maggior sensibilità;
Gadolinio;
Lunghi tempi d’attesa;
Poche apparecchiature sul territorio;
Maggior durata d’esecuzione;
Costi esorbitanti delle apparecchiature;
Numerose controindicazioni;
Spesso «manca» le microcalcificazioni; Falsi positivi e sovrastima;
Difficoltà nelle manovre interventistiche.
Contrasto mediante tomosintesi;
Risoluzione spaziale;
Radiazioni ionizzanti;
Maggiore specificità;
Mdc iodati;
Stessa seduta di una mx convenzionale;
Immagini seriate; Dispositivi meno costosi; Impossibilità di fare ricostruzioni in postprocessing.
Si riconferma la RM come indagine dall’elevata sensibilità e relativamente bassa specificità. La dual-energy ha dimostrato di eguagliare la RM nel rilevamento del ca. ma con meno falsi positivi quindi con una migliore specificità.
La dual-energy, a causa della sua minor sensibilità e dell’utilizzo di radiazioni ionizzanti, non può sostituire la RM. Si propone invece come alternativa poiché applicata alle stesse indicazioni ma più rapida e meno costosa, l’immagine è ricostruita da una acquisizione a bassa energia (25-29 kVp) e una ad alta energia (45-49 kVp) Mammografia digitale sottrattiva a doppia energia con mezzo di contrasto: dosi e immagini dal punto di vista fisico R. Sghedoni, M. Bertolini la tecnica è implementata su mammografi digitali GE richiede rapido cambiamento della tensione impostata (es. da 28 kV a 45 kV) filtro aggiuntivo in rame+alluminio rapida commutazione dei filtri l’elevata filtrazione nell’acquisizione ad alta energia richiede l’impostazione di valori di corrente elevati bassa energia spessore fantoccio anodo/filtro kV mAs 20 mm Mo/Rh 27 54 30 mm Mo/Rh 27 54 40 mm Mo/Rh 28 86 50 mm Rh/Rh 29 79 alta energia spessore fantoccio anodo/filtro kV mAs 20 mm Mo/Cu 46 98 30 mm Mo/Cu 46 98 40 mm Mo/Cu 45 152 50 mm Rh/Cu 45 218
La CESM appare davvero una metodica promettente nella diagnostica senologica di II° livello, non eseguibile cioè di routine, con costi e tempistiche ridotti ed un’ottima tollerabilità da parte della paziente». Consiste in una mammografia “contrastata” a livello delle aree di interesse interpretate in relazione all’intensità dell’impregnazione del m.d.c. e del relativo profilo morfostrutturale.
La metodica “cancella” il normale parenchima mammario per evidenziare le impregnazioni patologiche di m.d.c. corrispondenti alla sede della neo-vascolarizzazione tumorale (angiogenesi).
può essere usato per confermare i risultati e individuare le lesioni quando i risultati che emergono dallo screening non si dimostrano utili. L’esame richiede meno di 10 minuti e utilizza la stessa apparecchiatura, la stessa sala e lo stesso personale della mammografia
La CESM può essere utilizzata quando esiste un dubbio su una lesione diagnosticata con tecniche tradizionali (mammografia ed ecografia) permettendo, grazie all’assorbimento del mezzo di contrasto, di differenziare una lesione tumorale da una benigna. Tenuto conto di ciò, la CESM può essere utilizzata per le seguenti indicazioni: lesioni occulte, dubbie o sospette alla mammografia di base; diagnosi differenziali tra cicatrice e recidiva in paziente operata per carcinoma mammario; pazienti che debbano eseguire una stadiazione pre-chirurgica di una neoplasia nota e che presentino controindicazioni – relative o assolute – all’esecuzione di una risonanza magnetica (RM): claustrofobia, grave sovrappeso, dispositivi medici RM incompatibili; per la valutazione dell’estensione e della natura della patologia tumorale.
- Steven P. Poplack et all. Digital breast tomosynthesis: initial experience in 98 women with abnormal digital screening mammography. AJR:189, September 2007 • Hendrik J. Teertstra et all. Breast tomosynthesis in clinical practice: initialresults. Eur radiol (2010) 20:16- 24 • Mark A. Helvie et all. Digital mammography imaging:breast tomosynthesis and advanced applications. Radiol Clin North Am 2010 September; 48(5):917-929 • Comparison of digital mammography alone and digital mammography plus tomosynthesis in a population based screening program. Per Skaane M.D. et all. Radiology 2013 BACKGROUND TOMOSINTE
La ricostruzione a strati della tomosintesi riduce o elimina i problemi causati dalla sovrapposizione dei tessuti, anche se il limitato angolo di rotazione (rispetto alla rotazione di 360° della TC) non consente una completa cancellazione dei particolari contenuti nei piani sovra o sottostanti rispetto a quello di interesse (“ombre di trascinamento”). Tuttavia i particolari anatomici realmente presenti nel piano esaminato, appaiono perfettamente “a fuoco” e quindi con una evidenza (rapporto segnale/rumore) molto maggiore. TOMOSINTESI 3D (DBT) Negli ultimi anni in letteratura sono comparsi studi sulla tomosintesi Recenti sono gli studi sulla tomosintesi in screening, pochi pubblicati con casistiche limitate • Steven P. Poplack et all. Digital breast tomosynthesis: initial experience in 98 women with abnormal digital screening mammography. AJR:189, September 2007 • Hendrik J. Teertstra et all. Breast tomosynthesis in clinical practice: initialresults. Eur radiol (2010) 20:16- 24 • Mark A. Helvie et all. Digital mammography imaging:breast tomosynthesis and advanced applications. Radiol Clin North Am 2010 September; 48(5):917-929 • Comparison of digital mammography alone and digital mammography plus tomosynthesis in a population based screening program. Per Skaane M.D. et all. Radiology 2013 BACKGROUND
Consiste in una mammografia “contrastata” a livello delle aree di interesse interpretate in relazione all’intensità dell’impregnazione del m.d.c. e del relativo profilo morfostrutturale.
La metodica “cancella” il normale parenchima mammario per evidenziare le impregnazioni patologiche di m.d.c. corrispondenti alla sede della neo-vascolarizzazione tumorale (angiogenesi).
Può essere usata per confermare i risultati e individuare le lesioni quando i risultati che emergono dallo screening non si dimostrano utili. L’esame richiede meno di 10 minuti e utilizza la stessa apparecchiatura, la stessa sala e lo stesso personale della mammografia
SenoBright è il primo strumento al mondo a sfruttare i vantaggi della mammografia spettrale con miglioramento del contrasto (Contrast-Enhanced Spectral Mammography, CESM), una tecnica che si basa sulle acquisizioni a doppia energia. Grazie all’uso di un agente di contrasto iodinato e una dose di radiazioni bassa, SenoBright può offrire immagini morfologiche simili alle mammografie digitali standard e alle immagini con miglioramento del contrasto di alterazioni vascolari anomale intorno alle lesioni.
CESM vi offre più informazioni e vi aiuta a ottenere le risposte di cui avete bisogno quando i risultati di mammografie ed ecografie non si rivelano utili. SenoBright evidenzia un flusso sanguigno anomalo che può destare sospetto con un’immagine a bassa energia, che mostra la densità dei tessuti, e un’immagine con miglioramento del contrasto e soppressione del segnale di base.
“Abbiamo avuto un’ottima esperienza con la tecnica CESM, che ormai fa parte degli strumenti a nostra disposizione. A volte non abbiamo le risposte che vorremmo e temiamo che le conclusioni cui siamo giunti non siano corrette, soprattutto se la donna ha un tessuto denso che potrebbe nascondere dettagli importanti potenzialmente pericolosi […]”
Dott. Shroeder, Radiologo e Responsabile medico, Eastern Radiologists Inc., North Carolina
La tecnica CESM consente a tutti gli specialisti, chirurgo della mammella, medico referente o oncologo, di visualizzare l’immagine mammografica a cui sono abituati.
Semplicità di accesso.
L’esame con SenoBright CESM è simile a un normale esame mammografico e può essere eseguito in meno di dieci minuti. Non è limitativo per le pazienti che hanno difficoltà a sottoporsi ad altri test diagnostici per qualunque motivo, siano questi problemi economici, claustrofobia, peso, ritardi associati all’accesso e così via. Scoprite come si esegue un esame CESM.
L’utilizzo di mezzo di contrasto permette di evidenziare la proliferazione di vasi in prossimità del tumore (come in risonanza magnetica) si tentò inizialmente una strategia basata sulla sottrazione temporale (come in RM) di immagini ad alta energia la sottrazione temporale è stata abbandonata: la strategia oggi utilizzata (CESM) prevede l’acquisizione in rapida sequenza di una coppia di immagini a bassa ed alta energia dalla “sottrazione” delle due immagini si ottiene una visualizzazione del contrasto sviluppa vasi per il nutrimento delle cellule -> angiogenesi: processo fondamentale per la crescita della patologia da Pandya et al., Vascular Pharmacology,
“In caso di dubbi, comuni nell’oncologia mammaria e nell’imaging mammario, potete offrire [alle pazienti] uno strumento disponibile in sede […] che assicura risultati in 30 minuti”.
Dott. Suzette Delaloge, Head of the Breast Cancer Group presso l’Institut Gustave Roussy, Parigi, Francia
La tecnica CESM consente a tutti gli specialisti, chirurgo della mammella, medico referente o oncologo, di visualizzare l’immagine mammografica a cui sono abituati.
“La tecnica CESM è realmente utile per accorciare il ciclo [di diagnosi del tumore al seno] dalla diagnosi iniziale al trattamento chirurgico definitivo”.
Mammografia con miglioramento del contrasto
La mammografia con miglioramento del contrasto definisce aree della mammella associate a lesioni ipervascolarizzate dopo l’iniezione di un agente di contrasto iodinato.
I livelli di energia della mammografia convenzionale sono solo leggermente sensibili alla presenza di iodio nella mammella. Come mostrato nella Figura 1a, una concentrazione clinica atipica di iodio nella mammella determina un segnale a bassa intensità ed è difficilmente distinguibile dalla morfologia di base della mammella. Per ottenere immagini che evidenziano efficacemente la presenza di iodio, è stata proposta la cancellazione del tessuto mammario di base.
Per cancellare il tessuto mammario di base ed evidenziare le aree con iodio, è possibile utilizzare la mammografia spettrale con miglioramento del contrasto (CESM), una tecnica basata sulle acquisizioni a doppia energia dove due immagini vengono acquisite utilizzando spettri a raggi X a bassa energia (LE – valori di KV e filtrazione della mammografia standard) e ad alta energia (HE – valori KV più alti e maggiore potenza di filtrazione) (Figure 1a e 1b). Le differenze tra l’attenuazione dei raggi X di iodio e tessuti mammari a questi due livelli di energia vengono utilizzate per la soppressione del tessuto mammario di base (Figura 1c).
Figura 1. Illustrazione del principio della tecnica CESM su un fantoccio strutturato equivalente al tessuto mammario contenente dischi con concentrazioni cliniche di iodio tipiche. (a) L’immagine a bassa energia viene acquisita utilizzando i livelli di energia della mammografia standard. Lo iodio è difficile da rilevare. (b) L’immagine ad alta energia viene acquisita utilizzando un livello di energia medio superiore al limite K dello iodio. La rilevabilità dello iodio migliora, ma è comunque limitata dallo sfondo equivalente del tessuto strutturato. Questi alti livelli di energia, inoltre, comportano una riduzione del contrasto del tessuto mammario. (c) Nell’immagine dello iodio, il tessuto di base viene eliminato e lo iodio è facilmente visibile. (Gli elementi radiolucenti sono artefatti nel fantoccio.)
Un esame SenoBright può essere eseguito sull’apparecchiatura per mammografia immediatamente dopo una mammografia e/o un’ecografia standard. L’esame è molto simile alla normale mammografia, con l’eccezione dell’iniezione endovenosa, che viene somministrata come le iniezioni per gli esami TC, e richiede meno di 10 minuti. Dopo un’attesa iniziale di 2 minuti successivamente all’iniezione, SenoBright esegue le 4 viste standard (immagini ad alta e bassa energia) in 5 minuti (vedere la Figura 1).
Il sistema acquisisce automaticamente i dati spettrali necessari per creare automaticamente due immagini per ciascuna vista. La rapida acquisizione delle immagini è resa possibile dalla successione dinamica tra gli spettri a raggi X LE e HE, grazie alla rapida alternanza tra le tensioni dei tubi radiogeni e i filtri e alla rapidità di lettura del sensore.
La Figura 1 illustra un esame tipico con SenoBright. Viene innanzitutto iniettato un agente di contrasto iodinato mentre la paziente è comodamente seduta o distesa e con la mammella non compressa. In genere, due minuti dopo l’inizio dell’iniezione la mammella viene posizionata e compressa per la prima vista e viene acquisita la prima coppia di immagini. Subito dopo, il seno viene automaticamente decompresso. Vengono quindi acquisite altre tre coppie di immagini in modo simile per ottenere un esame bilaterale a due viste completo. In questo esempio, la durata totale di acquisizione delle immagini è pari a circa 5 minuti e la procedura totale si protrae per circa 7 minuti. La semplicità di utilizzo e la rapidità di esecuzione dell’esame creano un flusso di lavoro efficiente che mira a creare un’esperienza ottimale per la paziente.
Scoprite come si esegue un esame CESM..
“È sorprendente quanto sia semplice”. Earline W.
Abstract and Introduction
Introduction
Contrast-enhanced digital mammography (CEDM) takes sequential images at high and low energies that are used to construct a digitally subtracted image, highlighting areas of contrast medium enhancement. The low-energy image is of the same diagnostic quality as standard 2-dimensional mammography.[1] However, the digitally subtracted image is unlike those that mammographers are accustomed to interpreting and its use initially may be overwhelming.
With this paper, the authors aim to increase understanding of normal anatomic and non-anatomic structures encountered on subtracted images and increase awareness of commonly encountered artifacts. In addition, the authors outline a standardized reporting system to help further streamline interpretation and reporting of CEDM images.
What Is CEDM?
CEDM is a quick, well-tolerated, relatively low-cost breast imaging technique that combines standard full-field digital mammography (FFDM) with an intravenous, low-osmolar, iodinated contrast medium. After administration of contrast material in the antecubital vein, 2 sequential images are acquired at high and low energies. The low-energy image (26–32 kVp) yields soft tissue and calcification detail similar to standard FFDM;[2] the high-energy image (45–49 kVp) is specifically selected to be greater than the K-edge of iodine (33.2 keV).[3] These 2 images are then digitally subtracted from each other to produce a single contrast medium-enhanced image that highlights areas of neovascularity, similar to magnetic resonance imaging (MRI).
Numerous studies have demonstrated increased sensitivity and specificity of CEDM compared with either FFDM or FFDM combined with ultrasonography.[4] In addition, CEDM rivals the sensitivity of more costly and time-consuming examinations, such as MRI and molecular breast imaging.[5–9]
Dromain et al,[4] Jochelson et al,[5] Fallenberg et al,[3] and Luczynska et al[10] compared the sensitivity and specificity of CEDM with FFDM. In all 4 cohorts, CEDM showed greater sensitivity (93%-100%) and specificity (41%-85%) in the detection of breast cancer than FFDM (sensitivity, 78%-91%; specificity, 15%-58%). In 2011, Dromain et al[4] compared CEDM with FFDM and ultrasonography. They found that CEDM had a sensitivity of 93% vs a sensitivity of 90% for FFDM with ultrasonography, as well as improved specificity (63% for CEDM vs 47% for FFDM with ultrasonography). In a comparison of CEDM with MRI, 2 studies have shown that CEDM is similar to MRI. Jochelson et al[5] found that CEDM and MRI have equal sensitivity (96%), and Fallenberg et al[6] found CEDM to have 100% sensitivity compared with 97% sensitivity for MRI.
CEDM è una tecnica di imaging del seno relativamente a basso costo, ben tollerata, che combina la mammografia digitale standard a campo pieno (FFDM) con un mezzo di contrasto endovenoso, basso osmolato e iodato. Dopo la somministrazione del materiale di contrasto nella vena antecubale, vengono acquisite 2 immagini sequenziali ad alta e bassa energia. L’immagine a bassa energia (26-32 kVp) produce un dettaglio morbido e calcificato simile a quello standard FFDM; [ 2 ] l’immagine ad alta energia (45-49 kVp) è specificatamente selezionata per essere maggiore del bordo K di iodio (33,2 keV). [ 3 ] Queste 2 immagini vengono quindi sottratte digitalmente l’una dall’altra per produrre un’immagine a contrasto singolo a contrasto che evidenzia aree di neovascolarità, simile alla risonanza magnetica (MRI).
Numerosi studi hanno dimostrato una maggiore sensibilità e specificità del CEDM rispetto a FFDM o FFDM combinati con l’ultrasuono. [ 4 ] Inoltre, CEDM rivale la sensibilità degli esami più costosi e più lunghi, come la MRI e l’imaging molecolare del seno. [ 5-9 ]
Dromain ed altri, [ 4 ] Jochelson et al, [ 5 ] Fallenberg ed altri, [ 3 ]e Luczynska et al [ 10 ] hanno confrontato la sensibilità e la specificità del CEDM con FFDM. In tutte le 4 coorte, la CEDM ha mostrato una maggiore sensibilità (93% -100%) e specificità (41% -85%) nella rilevazione del cancro della mammella rispetto a FFDM (sensibilità, 78% -91%, specificità, 15% -58% . Nel 2011, Dromain et al [ 4 ]confrontato CEDM con FFDM e ultrasonografia. Hanno trovato che la CEDM ha avuto una sensibilità del 93% contro una sensibilità del 90% per FFDM con ultrasuoni e una maggiore specificità (63% per CEDM vs 47% per FFDM con ecografia). In un confronto tra CEDM e MRI, 2 studi hanno dimostrato che CEDM è simile a MRI. Jochelson ed altri [ 5 ] hanno rilevato che la CEDM e la MRI hanno la stessa sensibilità (96%) e Fallenberg ed altri [ 6 ] hanno trovato che la CEDM ha una sensibilità al 100% rispetto alla sensibilità del 97% per la RM.
Strutture anatomiche
Pelle . L’aspetto della pelle su un’immagine sottovolta CEDM può essere variabile (Figura 1). In primo luogo, la pelle non sta rafforzando o mostra una sottile linea di miglioramento. Raramente, mostra l’ispessimento artifactual non visto sulla immagine standard 2-dimensionale. Questo artefatto è pensato per essere correlato alle limitazioni del rilevatore di corrente per quanto riguarda le dosi di raggi X ad alta energia. Data l’aspetto variabile della pelle sulle immagini di sottrazione, qualsiasi risultato deve essere correlato con l’immagine a basso consumo energetico. La presentazione paziente di miglioramento e di ispessimento della pelle sulle immagini di sottrazione può differire e deve essere valutata sulla base dell’immagine mammografica standard a bassa energia.
(Ingrandisci immagine)
Figura 1.
Apparenza della pelle. (A) L’immagine obliqua di sottrazione mediolaterale illustra una sottile linea di miglioramento della pelle, che è una comune ricerca benigna. Le visioni craniocaudali a basso contenuto energetico (B) e sottrazione (C) mostrano l’ispessimento della pelle patologica e il miglioramento di un carcinoma mammario provato biopsia.
Nipple . La valorizzazione superficiale periferica del capezzolo è comunemente vista su MRI, attribuibile alla ricca alimentazione sanguigna del complesso areolare del capezzolo. [ 11 , 12 ]Al contrario, l’immagine di sottrazione di CEDM può produrre diverse apparenze del capezzolo. Il più comune è quello di nessun miglioramento. Occasionalmente, una sottile linea scura è visibile alla base del capezzolo non allungante, che può dare l’illusione di un sottile margine di miglioramento periferico. Un aspetto meno comune è un miglioramento minimo alla base del capezzolo. Nei pazienti con capezzoli piatti, un sottile bordo sottile di miglioramento può essere visto contiguo alla pelle adiacente. Le differenze nel miglioramento del capezzolo tra MRI e CEDM sono probabilmente secondarie a una combinazione dei differenti agenti di contrasto utilizzati e della compressione applicata con CEDM.
Come per i tipici FFDM, bisogna fare ogni sforzo per mettere il capezzolo nel profilo. Quando il capezzolo non è in profilo (Figura 2A) il capezzolo può essere scambiato per una massa migliorante all’interno del seno anteriore. Per confronto, un’immagine che mostra il capezzolo nel profilo consente una migliore rilevazione delle masse subareolari e aiuta a impedire che il capezzolo venga scambiato per una massa (Figura 2B). Quando le limitazioni impediscono il posizionamento del capezzolo nel profilo, è necessario utilizzare un indicatore BB per indicarne la posizione.
(Ingrandisci immagine)
Figura 2.
Nipple fuori profilo. (A) La vista di sottrazione mostra una massa con corrispondente miglioramento nel seno destro anteriore. Questo è stato pensato per rappresentare forse un capezzolo fuori profilo, imitando una massa crescente. (B) Vista craniocaudale con il capezzolo nel profilo, non confermando massa retroareolare.
Muscolo pectoralis . La maggior parte dei muscoli pectoralis non mostra miglioramenti sulle immagini sottratte. Tuttavia, una piccola percentuale (11%) delle immagini sottratte dimostra la delineazione pettorale, che imita il miglioramento debole (Figura 3). La delineazione pettorale è un artefatto attribuito al movimento del paziente e non indica l’infiammazione o il cambiamento patologico all’interno del muscolo stesso. Pertanto, un artefatto di errori di registrazione, simile a quello osservato in MRI con il movimento del paziente, può essere presente quando si vede il contorno pettorale.
(Ingrandisci immagine)
Figura 3.
Aspetto pettorale. L’immagine obliqua di sottrazione mediolaterale mostra la delineazione pettorale.
Vascelli . Le imbarcazioni si esaltano maggiormente e si lavano alla prima vista rispetto alle viste successive, simili ai risultati della MRI (Figura 4). Anche simile alla MRI, quando il tumore al seno è presente, la neoangiogenesi provoca un aumento del numero di vasi che aumentano il seno affetto. [ 13 ]
(Ingrandisci immagine)
Figura 4.
Imbarcazioni. Simile a quella di risonanza magnetica, le immagini sottratte mostrano vasi avanzati. Sottrazione immagini oblique mediolaterali mostrano tipici vasi di espansione sulla destra. L’immagine sinistra mostra un seno con un miglioramento del carcinoma a prova di biopsia con angiogenesi associata. Da notare, si nota anche un linfonodo ascellare che aumenta notevolmente.
Nodi linfonodi . Anche se i linfonodi sono più frequentemente presenti nell’asse, i linfonodi intramammari possono essere osservati fino al 47% dei seni. [ 14 ] Questi risultati sono tipicamente riscontrati nei quadranti esterni superiori. I linfonodi normali ascellari e intramammari presentano caratteristiche apparentemente benigne, compresi i margini circoscritti; forma ovale, rotonda o reniforme; un grasso grigio; e la vicinanza a una nave.
Lymph nodes show various degrees of enhancement on CEDM images whereby the enhancement is not necessarily indicative of pathologic characteristics. Similar to MRI, normal lymph nodes may enhance avidly, whereas abnormal lymph nodes may not enhance at all.[15] Evaluation of lymph node size and morphologic characteristics, as well as assessment of stability over time, is essential. Abnormal lymph nodes may show a more rounded appearance because the typical nonenhancing hilum becomes replaced by tumor. The enhancement pattern usually becomes more heterogeneous with increased lymph node size and may be secondary to metastatic implants or areas of necrosis.
Migliorare le lesioni cutanee . Le lesioni cutanee con aumento della vascolarità, in particolare gli angiomi di ciliegia, possono dimostrare un miglioramento del contrasto sulle immagini CEDM e il cancro mimico. Tuttavia, nella nostra esperienza, i moli tipici ei cheratosi seborrhei non aumentano. Un esempio dell’importanza di mettere marcatori di mole sulla potenzializzazione delle lesioni cutanee è mostrato in Figura 5.
(Ingrandisci immagine)
Figura 5.
Miglioramento del mole. (A) L’immagine sinistra di craniocaudazione sinistra mostra una piccola area ovale di aumento (freccia) nel seno mediale e posteriore. Sull’esame ulteriore dell’immagine a basso consumo energetico, un bordo di aria sembra circondare una densità ovale in questa zona, suggestiva di una lesione cutanea. (B) Ripetere l’immagine craniocaudale bidimensionale del seno sinistro presa dopo l’inserimento di un marker di mole, confermando che la lesione ovale aumentante corrispondeva ad un angioma ciliegio.
Strutture non anatomiche
Clips. La posa delle clip dopo la biopsia del seno è comune. Gli oggetti altamente attenuati, come le clip e le calcificazioni, possono mostrare un’aspetto variabile. Questa variazione dipende da una funzione demetale che è intrinseca al software CEDM (Hologic, Inc). Quando la funzione demetale è spenta, le clip e le calcificazioni appaiono scure; nella posizione abilitata, queste strutture appaiono luminose. Attualmente, poiché gli artifici possono essere causati dalla funzione demetal, l’impostazione predefinita all’interno del sistema Hologic è la posizione off. Gli aggiornamenti futuri del software hologico dovrebbero risolvere questi manufatti e consentire la funzionalità demetale di rimanere, conferendo clip e calcificazioni l’aspetto luminoso di cui la maggior parte dei mammografi sono abituati. Un terzo tipo, quello di alternare apparenza brillante e scura, dà un artefatto zebra ed è secondario a una registrazione errata che causa il movimento (Figura 6)(Ingrandisci immagine)
Manifesto di errori di registrazione. La sottrazione delle immagini da due pazienti mostra un manufatto di errori. Le clip chirurgiche visualizzate sull’immagine di sottrazione del pannello sinistro presentano linee luminose e scure a fianco a fianco, causando così il cosiddetto artefatto zebra dalla registrazione errata. L’artefatto di Zebra è presente anche nel pannello destro, sull’immagine di sottrazione di una calcificazione distrofica.
Calcificazioni . Poiché la funzione demetal è in default alla posizione off, la maggior parte delle calcificazioni sono scure nelle immagini sottratte. Tuttavia, le microcalcificazioni (<0,5 mm) visualizzate sull’immagine a basso consumo energetico sembrano occultate, senza oscurità (Figura 7) o aspetto luminoso. In alcuni casi in cui la funzione di demetalizzazione è stata accesa inavvertitamente tra le viste, le calcificazioni appaiono scure su una vista ma luminose sull’altra vista. Le calcificazioni più grandi non possono apparire uniformemente oscure quando è presente la registrazione errata (Figura 6, pannello a destra). Per questi motivi, è importante utilizzare le immagini a basso consumo energetico per valutare i seni per microcalcificazio
Calcificazioni. Una calcificazione rotonda (freccia) mostra l’aspetto oscuro atteso sull’immagine di sottrazione.
artefatti
Registrazione errata . Dato che le immagini ad alta energia e bassa energia vengono acquistate subito dopo l’altra, il potenziale di movimento esiste e può causare un errore di registrazione. La scorrimento tra le due immagini provoca aree adiacenti scure e luminose, causando così il cosiddetto artefatto zebra. Questo artefatto è stato visto legato a clip, vasi e calcificazioni (Figura 6).
Air Gap e altri artefatti ad alta attenuazione . Nella nostra esperienza con il CEDM, l’artefatto più comune deriva da un traferro d’aria. Il contatto parziale tra la pelle e il rivelatore o la paddle di compressione crea un artefatto scuro che prende la configurazione di un’area di contatto incompleto. Il contatto imperfetto può provocare compressioni improprie, sfregamento della pelle o piegature della pelle (Figura 8). Simile alle clip e alle calcificazioni, si può vedere un aspetto scuro di aureo attorno ad altri elementi ad alta attenuazione, come marcatori a strisce, marcatori delle cicatrici, marcatori BB, pacemaker e porti di petto secondari a un artefatto di elaborazione delle immagini.
(Ingrandisci immagine)
Figura 8.
Manufatti aggiuntivi. Il contatto incompleto della pelle con la paga crea lacune di aria, causando un artefatto scuro. (A) mostra un vuoto d’aria nel seno medio sinistro. (B) mostra un artefatto curvilineo scuro con la piega della pelle del seno superiore sinistro e del tessuto ascellare. Inoltre, è rappresentata un’alone scuro, risultante da un artefatto di elaborazione delle immagini, che circonda l’indicatore di mole.
Contrasto Contaminazione . Il materiale di contrasto esterno al paziente, come sulla pelle, la pagaia o il rivelatore, può causare artefatti luminosi sovrapposti. In un esame CEDM, la precauzione è fondamentale per prevenire la contaminazione. La figura 9 mostra un caso inizialmente presumibile per avere aree multiple e bilaterali di aumento anormale. Su un’ulteriore revisione delle immagini, le aree di supposta miglioramento mostravano una configurazione di immagine a specchio che suggeriva la contaminazione del contrasto della pala o del rivelatore o entrambi.
(Ingrandisci immagine)
Figura 9.
Contrasto contaminazione. Le immagini craniocaudali sottrattate a destra e sinistra mostrano diverse aree di aumento della massa non in massa in entrambi i seni (frecce e parentesi). A seguito di ulteriori esami, le aree esaminate di presunto miglioramento nel seno destro sono esatta immagini speculari di quelle del seno sinistro. Ad esempio, la piccola area di presunto miglioramento del seno mediale destro, profondità anteriore (A, staffa) corrisponde ad una simile area di miglioramento nel seno laterale sinistro, profondità anteriore (B, staffa e frecce). La natura dello specchio-immagine del presunto miglioramento suggerisce la contaminazione esterna del mezzo di contrasto della pagaia e del rivelatore.
Valutazione e segnalazione CEDM
Non è stato stabilito alcun metodo di reporting per le immagini CEDM sottrae ad alta energia. La nostra istituzione ha adottato un sistema di reporting standardizzato attraverso il lessico Breast Imaging-Reporting e Data System (BI-RADS), simile a quelli già pubblicati per la mammografia, l’ultrasuono e l’MRI. [16 ]
L’immagine a bassa energia viene interpretata come una scansione mammografica standard. La densità del seno, cioè quasi completamente grassi, aree sparse di densità fibroglandolari, eterogeneamente dense o estremamente dense) [ 16 ] è inclusa nella relazione, oltre a risultati rilevanti di immagini.
La sezione successiva del rapporto CEDM descrive i risultati sull’immagine sottratta. Lo sfondo di miglioramento parenchimale (BPE) è descritto in 1 delle 4 categorie (simile a BI-RADS MRI BPE): minimo, lieve, moderato e marcato (Tabella e Figura 10). Il BPE minimo è definito come valorizzazione dello 0% al 24%; lieve come miglioramento del 25% al 49%; moderato come miglioramento del 50% al 74%; e contrassegnato come miglioramento generalizzato diffuso del 75% al 100%.
(Ingrandisci immagine)
Figura 10.
Miglioramento della priorità bassa. I rapporti mammografici digitali migliorati a contrasto devono includere il grado e la simmetria del miglioramento della priorità bassa. Le sottrazioni di immagini da tre pazienti mostrano un miglioramento parenchimale di sfondo (A), lieve (B), moderato (C) e marcato (D).
Simile a MRI, l’aumento del BPE può comportare un aumento delle tariffe di richiamata. Il BPE è classificato come simmetrico o asimmetrico tra i seni e, simile a quello della RM, può essere visto un aumento asimmetrico a causa di cause benigne e maligne, incluse quelle in pazienti con storia di trattamento radiologico o manifestazione patologica estesa in un solo seno (Figura 11). [ 17 ]
(Ingrandisci immagine)
Figura 11.
Miglioramento asimmetrico della priorità bassa. Le immagini di sottrazione presentano un miglioramento asimmetrico: lieve sul seno sinistro (A) e moderato sul seno destro (B).
I risultati descritti su mammografia a bassa energia, quali calcificazioni, asimmetrie e masse, vengono ulteriormente valutate per eventuali aree corrispondenti di aumento anormale sulle immagini sottratte. Le aree di aumento anormale sono descritte ulteriormente come aumento di massa o di massa .
Il termine ” aumento di massa” è usato per descrivere una lesione che occupa spazio con bordi di massa; il termine ” non-mass enhancement” descrive un’asimmetria senza frontiere chiare. [ 16 ] La determinazione della valorizzazione di massa o di massa non è meglio effettuata attraverso l’interrogazione dell’immagine a basso consumo in combinazione con l’immagine sottratta, in quanto la forma ei margini sono spesso meglio delineati sull’immagine a basso consumo energetico. Le migliorie di massa e di massa non sono descritte dalla loro posizione del quadrante e date una misurazione tridimensionale.
Inoltre, le aree di miglioramento della massa sono descritte dal loro modello di miglioramento, compreso omogeneo, eterogeneo o che aumenta il bordo. Il grado di aumento di massa o di massa non è documentato utilizzando una delle 4 categorie: nessuna, lieve, moderata o marcata. Infine, sono riportate osservazioni pertinenti riguardanti le strutture al di fuori del parenchima del seno (es. Axilla, pelle, capezzolo) (Figura 12).
Miglioramento delle lesioni. I rapporti mammografici digitali avanzati dovrebbero includere il grado di miglioramento delle lesioni. La sottrazione di immagini da due diversi pazienti mostra diversi gradi di valorizzazione. (A) La lesione anteriore (freccia gialla) mostra un lieve aumento e corrisponde ad un hamartoma provato da biopsia. La lesione posteriore (freccia rossa) mostra una moderata valorizzazione ed è stato un carcinoma duttale invasivo bioptico-provato. (B) Il miglioramento evidenziato può essere visto nel grande carcinoma duttale invasivo del dente superiore superiore.
Conclusioni
CEDM è una nuova modalità che continua a mostrare una maggiore sensibilità nel rilevamento del cancro al seno rispetto alla mammografia standard. Gli studi riportati in letteratura continuano a misurare la performance del CEDM rispetto alla mammografia standard, alla MRI e ad altre modalità di mastoplastica. Forniamo la prima guida, a nostra conoscenza, per radiologi e clinici nell’interpretazione delle immagini sottrattate a contrasto. Nel fornire esempi di casi relativi agli artefatti anatomici e non anatomici nella nostra pratica, speriamo di facilitare la transizione e di risolvere eventuali problemi che possono sorgere durante l’interpretazione iniziale. Viene offerta una struttura di reporting basata su BI-RADS per consentire rapporti costanti e basati sulla qualità per i medici.
Precisione del CESM rispetto alla mammografia convenzionale ed agli ultrasuoni nella valutazione di BI-RADS 3 e 4 lesioni del seno con correlazione patologica
Autore link pannello sovrapprezzoMaha Helal aManal F. Abu Samra bMohammed A. Ibraheem bAsmaa Salama cEbtesam Esmail Hassan dNour El-Huda Hassan b
Mostra di più
https://doi.org/10.1016/j.ejrnm.2017.03.004Ottieni diritti e contenuti
Open Access finanziato dalla Società egiziana di Radiologia e Medicina Nucleare
Creative Commons licenza
Scopo
Valutare l’accuratezza della mammografia spettrale migliorata in contrasto (CESM) rispetto alla mammografia e ultrasuoni convenzionali nella valutazione di BI-RADS 3 e 4 lesioni mammarie con correlazioni patologiche.
Pazienti e metodi
Trenta pazienti di sesso femminile con 35 lesioni al seno diagnosticate con l’imaging convenzionale come BI-RADS 3 e 4, presentate all’Unità di radioterapia femminile tra gennaio e dicembre 2015, hanno un’età variabile da 23 a 70 anni. Tutti i pazienti sono stati sottoposti a mammografia convenzionale e ultrasuoni poi CESM.
Risultati
I pazienti sono divisi in due gruppi, gruppo lesioni benigne e maligne secondo l’analisi istologica. Il risultato della mammografia è che le lesioni maligne sono state rilevate in 18/35 (51,4%) mentre le lesioni benigne sono 17/35 (48,6%). L’ultrasuono ha rivelato 27/35 (77,1%) lesioni erano maligne e 8/35 (22,9%) le lesioni benigne. Ma CESM, ha rivelato 25/35 (71,4%) lesioni erano maligne e 10/35 (28,6%) le lesioni benigne. Tra i 7 pazienti con lesioni maligne multifocali / multicentriche istologicamente comprovate, tutte rilevate da casi CESM 7/7 (100%) contro 2/7 casi (28,6%) e 6/7 casi (85,7%) rilevati rispettivamente dalla mammografia e dall’ecografia . Basandosi su, CESM aveva una sensibilità del 95,2% e un’accuratezza diagnostica del 82,9%.
Conclusioni
CESM ha una migliore esattezza diagnostica rispetto alla mammografia da solo e alla mammografia con ultrasuoni. CESM ha un’accuratezza diagnostica del 82,9% rispetto al 51,4% per la mammografia e al 77,1% per l’ultrasuono.
parole
Lesioni del seno
CESM
BI-RADS lessico
1 . introduzione
Il cancro al seno è il cancro più grave per la quale è diagnosticata la vita nelle donne in tutto il mondo [1] . È il 22,9% di tutti i nuovi tumori femminili e considerato il cancro più comune tra le donne sia nei paesi sviluppati che nei paesi in via di sviluppo. Il cancro al seno rappresenta il 37,7% del totale dei nuovi casi di cancro ed è la causa principale della mortalità correlata al tumore che rappresenta il 29,1% delle morti correlate al cancro nell’Egitto 2008 [2] .
L’aumento della consapevolezza pubblica e la migliore screening hanno portato alla diagnosi precoce a fasi atte a completare la resezione chirurgica e le terapie curative. Di conseguenza, i tassi di sopravvivenza per il cancro al seno sono notevolmente migliorati [3] . L’individuazione precoce del cancro al seno diventa un lavoro molto importante per ridurre la morbilità e la mortalità associata, quindi se viene effettuata attraverso esami regolari di cancro al seno in una fase precedente di quanto è attualmente possibile, il tasso di sopravvivenza entro 5 anni aumenterebbe a circa il 95% [4 ] .
Per la rilevazione del cancro al seno, la mammografia è una tecnica di imaging ben consolidata e conveniente [5] . Nonostante i progressi della mammografia, almeno uno su quattro tumori maligni rimane inosservato usando solo la mammografia di screening. Nel tessuto denso del seno, più della metà non è rilevato [6] . La mammografia ha una bassa sensibilità e specificità nelle donne con un seno radiografico denso, a causa del contrasto diminuito tra un possibile tumore e il tessuto del seno circostante e la somma dei tessuti può oscurare le lesioni [7] .
Gli sviluppi digitali in mammografia digitali a pieno campo hanno consentito una risoluzione rapida e più elevata del contrasto, una gamma dinamica migliorata e una rapida elaborazione di dati e immagini rispetto alla mammografia a film da schermo. Tuttavia, alcune limitazioni persistono [8] .
Due tecniche promettenti che possono superare le limitazioni della mammografia digitale sono la mammografia e la tomosintesi, una tecnica trasversale [9] .
La mammografia spettrale migliorata di contrasto è una nuova tecnica di imaging del seno che mira a dimostrare l’angiogenesi del carcinoma mammario. Sono stati acquisiti esperimenti tecnici e clinici e negli ultimi anni sono stati pubblicati risultati incoraggianti sul CESM in aggiunta alla mammografia [10] . È stato dimostrato che CESM migliora la probabilità di malignità e valutazione di BIRADS rispetto alla mammografia convenzionale da solo. CESM dovrebbe essere un utile complemento alla mammografia diagnostica e ad un promettente soluzione dei problemi e uno strumento di staging [8] .
La mammografia da solo e la mammografia in associazione con l’ultrasuono avevano meno precisione nel rilevamento del carcinoma mammario rispetto al CESM a doppia energia [5] . Come la MRI del seno, la CESM dovrebbe essere di particolare interesse per la valutazione dell’ampiezza della malattia in quanto consente una migliore valutazione della dimensione della lesione e la rilevazione di più tumori multifocali e multicentrici di mammella rispetto alla mammografia da solo o combinati con l’ecografia [7] . Per quanto riguarda la MRI contrast-enhanced, che è attualmente la tecnica più sensibile per il rilevamento del cancro al seno, ha ancora una bassa disponibilità, elevati costi e un elevato tasso di falsi positivi [5] . La tecnica di imaging veloce con disponibilità immediata nella suite mammografica senza un nuovo appuntamento ha considerato il vantaggio di CESM[5] .
Lo scopo di questo studio era quello di valutare l’accuratezza della Mammografia Spectral Enhanced Contrasto contro la Mammografia Convenzionale e l’Ultrasuono nella Valutazione di BI-RADS 3 e 4 lesioni del seno con correlazione patologica.
2 . Pazienti e metodi
2.1 . Coorte di studio
Tra gennaio e dicembre 2015 sono stati inclusi trenta pazienti femminili con 35 lesioni al seno (BIRADS 3 & 4) sull’immagine convenzionale, con l’analisi patologica come riferimento di riferimento. L’età dei partecipanti varia dai 23 ai 70 anni, con età media ± sd 46,8 ± 11,9. Tutti i pazienti sono stati sottoposti a esame clinico e immagini convenzionali (mammografia convenzionale e ultrasuono). Sono state fatte spiegazioni dettagliate sulle procedure per tutti i pazienti, inclusi i rischi associati e le controindicazioni. Il comitato etico istituzionale ha approvato questo studio e condotto con consenso informato.
2.2 . Procedure di imaging
Tutti i pazienti sono stati sottoposti a mammografia convenzionale e ultrasuoni al seno, quindi tutti i casi sono stati sottoposti a contrastare la mammografia spettrale migliorata. Criteri di inclusione, tutti i pazienti con BIRADS 3 & 4 lesioni al seno sulle immagini convenzionali (mammografia convenzionale e ultrasuono). Criteri di esclusione, controindicazione all’iniezione endovenosa del materiale di contrasto (pazienti allergici o quelli conosciuti per avere storia di complicazione da mezzi di contrasto quali reazioni anafilattiche). Pazienti con insufficienza renale o lesioni e pazienti con cattive condizioni generali.
2.3 . attrezzatura
Gli studi di mammografia avanzati di contrasto sono stati eseguiti utilizzando GE Senographe 2000D sistema di mammografia digitale full-field di GE Healthcare, Chalfont St-Giles, Regno Unito. Utilizzava un sistema di mammografia digitale a campo pieno utilizzando un rivelatore a piastra con CsI assorbitore, dimensione campo 19 × 23, del pitch di 100 mm, formato matrice immagine 1914 × 2294 (Senographe DS), con alcuni adattamenti software e hardware specifici per acquisizione e elaborazione delle immagini. I pazienti sono stati esaminati con un dispositivo a ultrasuoni utilizzando la macchina ad ultrasuoni (Logiq P5, GE Medical Systems, Corea) con un trasduttore lineare da 7,5-12 MHz.
2.4 . Tecnica della mammografia spettrale a doppia energia a pieno campo
Uso di agente di contrasto non ionico, omnipaque 300; Nycomed, Roskilde, Danimarca, iniezione di 1,5 ml / kg di peso corporeo, è stata eseguita una dose intravenosa con iniezione manuale. Due minuti dopo l’avvio di somministrazione di agenti contrastanti; sono state eseguite due esposizioni energetiche basse ed elevate, il seno di preoccupazione è stato compresso in posizione CC, poi l’altro seno. Quindi visualizza il seno di preoccupazione nella posizione MLO e nell’ultima vista di un altro seno in posizione MLO, al fine di generare due immagini sottratte con informazioni sull’assorbimento del contatore di contrasto (una nella MLO e una nella visualizzazione CC).
2.5 . Analisi e interpretazione delle immagini
–
Per quanto riguarda l’esame mammografico, le lesioni sono state valutate per quanto riguarda la densità del seno in base al lessico di Breast Imaging Reporting e Data System (BI-RADS) progettato dall’American College of Radiology (ACR), luogo delle lesioni, tipo (massa, distorsione architettonica, asimmetria focale), margine, definizioni e ± calcificazioni.
Questo studio include 30 pazienti con 35 lesioni mammarie, età dei pazienti varia dai 23 ai 70 anni con un’età media di 46,8 ± 11,9 (media ± SD), 21 di essi erano maligni (BI-RADS 4) mentre 14 erano benigni ( BI-RADS 3) mediante istopatologia.
Risultati della mammografia sul punteggio ACR della densità del seno risulta che 8/35 (22,9%) casi sono stati assegnati un punteggio ACR 1, 11/35 (31,4%) casi erano ACR punteggio 2, 10/35 (28,6%) casi erano ACR dei casi 3 e 6/35 (17,1%) sono stati assegnati un punteggio ACR di 4, secondo la densità del seno di ACR BIRADS.
Classificazione mammografica delle lesioni del seno ( Tabella 1 ).
Tabella 1 . Classificazione mammografica delle lesioni del seno (N, 35).
| Risultati mammografici | No di lesione | % |
| Masse | 19 | 54,3% |
| Asimmetria focale | 12 | 34,3% |
| Massa e calcificazione | 3 | 8,6% |
| Asimmetria focale e calcificazione | 1 | 2,9% |
I risultati della mammografia sono stati lesioni maligne, BI-RADS 4 rilevate in 18/35 (51,4%) mentre lesioni benigne, BI-RADS 3 sono state rilevate in 17/35 (48,6%). Indici diagnostici di mammografia tra questo studio, correlati alle diagnosi finali ( Tabella 2 ).
Tabella 2 . Indici diagnostici di mammografia correlati con le diagnosi finali (per patologia).
| mammografia | Diagnosi finale | Diagnosi finale | Totale |
| Maligno | 11 (BI-RADS 4) (a) | 7 (BI-RADS 3) (b) | 18/35 |
| benigno | 10 (BI-RADS 4) (c) | 7 (BI-RADS 3) (d) | 17/35 |
| Totale | 21 (a + c) | 14 (b + d) | 35 (a + b + c + d) |
Sulla base dei precedenti risultati, la mammografia ha una sensibilità del 52,4%, una specificità del 50%, un valore predittivo positivo del 61,1% (PPV), un valore predittivo negativo del 41,1% (NPV) e l’accuratezza diagnostica del 51,4%.
Le ultrasuoni del seno sono state 28/35 (80%) lesioni presentate da lesioni di massa, mentre 7/35 (20%) presentate da lesioni non masse.
Per quanto riguarda la forma della massa, ovale o arrotondato è stato osservato in 12 lesioni mentre forma irregolare osservata in 16 lesioni da 28 lesioni. In questo studio 8/28 (28,6%) masse erano ben definite mentre 20/28 (71,4%) masse erano mal definite. L’echogenicità più comune delle lesioni era ipoecogena, come si nota al 19/28 (67,9%). La maggior parte delle lesioni 23/28 (82,1%) non mostrava alcun miglioramento posteriore né ombra.
PAROLE CHIAVE:
Neoplasie al seno; mammografia; Imaging, tridimensionale; Screening di massa; Dosaggio delle radiazioni; Analisi costo-efficacia; Valutazione della tecnologia; biomedica