Intelligenza artificiale e mammografia

Probabilmente l’Intelligenza Artificiale potrà fare meglio di noi quando si tratta di diagnosi. Studi condotti negli Stati Uniti hanno evidenziato che, grazie agli algoritmi di deep learning su cui si basa l’Intelligenza Artificiale, è possibile ottenere una riduzione assoluta del 5,7% dei falsi positivi e del 9,4% di quelli negativi. Inoltre nel confronto con l’operato di 6 radiologi, è stato dimostrato un aumento dell’11,5% della sensibilità. Sono oltre 20mila le variabili nella pratica clinica per rendere le diagnosi di tumore della mammella più precise e poter così assumere decisioni ‘su misura’ sul trattamento di precisione. Tutti obiettivi non raggiungibili da parte degli operatori sanitari con gli strumenti tradizionali. Le numerose applicazioni dell’Intelligenza Artificiale nella diagnosi e terapia della neoplasia del seno sono già realtà nei principali centri di riferimento del nostro Paese. “Oggi, in Italia, vivono più di 834mila donne dopo la diagnosi di tumore del seno, con una sopravvivenza a 5 anni che raggiunge l’88% – spiega Francesco Cognetti, presidente di Foce (Federazione degli oncologi, cardiologi e ematologi) e di Fondazione Insieme Contro il Cancro. Dal 2015 al 2021, è stata stimata una riduzione dei decessi pari quasi al 7%”. Un risultato molto importante, ottenuto grazie ai programmi di screening, che consentono di individuare la malattia in fase iniziale, e a terapie sempre più efficaci.
Secondo i dati dell’American Cancer Society circa il 13% della popolazione svilupperà un tumore al seno invasivo nella sua vita e il 3% (una donna su 39) morirà a causa della malattia. Sottoponendosi regolarmente a mammografie si può ridurre in modo significativo il rischio di mortalità per tumore al seno. L’IA potrebbe trovare applicazione per superare dei limiti in mammografia. Gli algoritmi dell’intelligenza artificiale possono analizzare immagini diagnostiche e fornire approfondimenti diagnostici superando delle criticità diagnostiche. ad esempio:
1) Alcuni casi di cancro al seno non sono identificati attraverso lo screening;
2) Eccessivi richiami per ulteriori test aggiuntivi;
3) Bassa sensibilità nei seni densi;
4) Variabilità inter-lettore.
5) È stato dimostrato che i sistemi di intelligenza artificiale possono migliorare le prestazioni dei radiologi e fornire risultati equivalenti o superiori a quelli dei soli radiologi.
Dall’insieme dei dati derivanti dalle tecnologie di sequenziamento l’IA può arrivare a comprendere meglio sviluppo e progressione del tumore della mammella. L’IA potrebbe essere di valido aiuto nella valutazione dei fattori di rischio.
LO STUDIO SCREENTRUSTCAD
Karin Dembrower, del Karolinska Institute, e i suoi colleghi svedesi in collaborazione con lo ScreenTrustCAD Trial Consortium hanno compiuto uno studio prospettico per valutare se la doppia lettura delle immagini mammografiche da parte dell’intelligenza artificiale e di un radiologo possa portare all’individuazione di più casi di cancro rispetto a quanto accada con la doppia lettura da parte di due radiologi.
Lo studio ha arruolato 55.581 donne di età compresa tra 40 e 74 anni (età media 55 anni) che si sono sottoposte a screening mammografico tra l’1 aprile 2021 e il 9 giugno 2022. L’outcome primario dello studio era la diagnosi tramite screening di cancro al seno entro 3 mesi dalla mammografia. È stato esaminato l’effetto delle seguenti combinazioni: doppia lettura condotta da un solo radiologo e dall’intelligenza artificiale (IA) confrontata con la consueta doppia lettura condotta da due radiologi, e lettura singola compiuta dall’IA rispetto alla lettura tripla eseguita da due radiologi più l’AI sempre confrontate con la doppia lettura standard condotta da due radiologi.
Ai fini dello studio, l’IA è stata implementata come lettore indipendente e, per ciascuna immagine, il sistema di IA ha generato un punteggio continuo in base al grado stimato di anomalia.
I risultati
A 269 (0,5%) donne totali è stato diagnosticato un carcinoma mammario rilevato sulla base di una prima lettura positiva della mammografia. Entrando nel dettaglio dell’analisi, la doppia lettura effettuata da un radiologo e dall’IA è risultata non inferiore per la rilevazione del tumore rispetto alla doppia lettura effettuata da due radiologi [261 (0,5%) casi rilevati rispetto ai 250 (0,4%) dei due radiologi].
Anche la lettura singola tramite IA [246 (0,4%) casi rilevati rispetto ai 250 (0,4%) dei due radiologi] e la tripla lettura effettuata da due radiologi più l’IA [269 (0,5%) casi rilevati sempre rispetto ai 250 (0,4%) dei due radiologi] sono risultate non inferiori alla doppia lettura effettuata da due radiologi.
La doppia lettura da parte di un radiologo più l’IA ha comportato un aumento del 4% (11/250) nella diagnosi del tumore al seno e un aumento del 21% nel numero di esami con interpretazione anomala.
Questo potrebbe suggerire che l’IA e i lettori ‘umani’ percepiscano caratteristiche dell’immagine leggermente diverse in caso di sospetto di cancro; pertanto, un lettore umano e l’IA potrebbero rappresentare una potenziale sinergia in termini di aumento della sensibilità per rilevare i tumori al seno. Le discussioni consensuali che hanno accompagnato in questo studio l’esame di tutte le mammografie hanno prodotto un tasso di richiamo inferiore del 4% (73/1629) nel caso di doppia lettura da parte di un radiologo più l’IA rispetto alla doppia lettura da parte di due radiologi. La discussione consensuale sembrerebbe quindi efficace nel garantire che il tasso più elevato di interpretazioni anomale ottenute con la doppia lettura da parte di un radiologo e l’IA non si traduca in un aumento del tasso di richiamo. Secondo gli autori l’IA è pronta per un’implementazione controllata, che includerebbe la gestione del rischio, la sorveglianza post-commercializzazione e il follow-up sistematico delle prestazioni nel mondo reale. Tuttavia gli autori sottolineano anche che attualmente non esistono protocolli sulla qualità dei dati delle prestazioni effettuate tramite l’IA.
Lo screening mammografico supportato dall’intelligenza artificiale è sicuro. Primo studio prospettico randomizzato su ‘Lancet Oncology’
Il lavoro è stato condotto in Svezia. Gli esperti dovranno ora verificare ora se questi risultati promettenti reggono in altre condizioni, ad esempio con altri radiologi o altri algoritmi di intelligenza artificiale.
Lo screening mammografico supportato dall’intelligenza artificiale (AI) è un’alternativa sicura alla pratica della doppia lettura da parte dei radiologi e può contribuire a ridurre i pesanti carichi di lavoro per i medici. La dimostrazione arriva da un’analisi ad interim di uno studio prospettico randomizzato controllato, che ha approfondito la sicurezza clinica dell’utilizzo dell’AI nello screening mammografico. Lo studio, condotto da ricercatori dell’Università di Lund in Svezia, è stato pubblicato su The Lancet Oncology.
Ogni anno circa un milione di donne in Svezia sono chiamate allo screening mammografico. In questo Paese, ogni esame di screening viene rivisto da due radiologi senologici per garantire un’elevata accuratezza del referto, con la cosiddetta ‘doppia lettura’. Vi è tuttavia una carenza di forza lavoro nel campo della radiologia senologica, in Svezia e anche altrove, che può ingolfare il servizio di screening. Le potenzialità dell’intelligenza artificiale per supportare lo screening mammografico ha attirato molta attenzione, ma come questa debba essere impiegata in modo ottimale e quali saranno le conseguenze cliniche, non è ancora chiaro.
Lo studio Mammography Screening with Artificial Intelligence (MASAI) è il primo studio controllato randomizzato che valuta l’efficacia dello screening supportato dall’intelligenza artificiale. “Nel nostro studio, abbiamo utilizzato l’intelligenza artificiale per identificare gli esami di screening ad alto rischio di cancro al seno, che sono stati sottoposti a doppia lettura da parte dei radiologi. I restanti esami sono stati classificati come a basso rischio e sono stati letti solo da un radiologo. Nella lettura dello schermo, i radiologi hanno utilizzato l’intelligenza artificiale come supporto per il rilevamento, in cui essa ha evidenziato risultati sospetti sulle immagini”, afferma Kristina Lång, ricercatrice e professoressa associata in radiodiagnostica presso l’Università di Lund e consulente presso lo Skåne University Hospital, che ha guidato lo studio.
Le 80.033 donne incluse nell’analisi di sicurezza sono state assegnate in modo casuale in due gruppi: 40.003 donne nel gruppo di intervento che sono state sottoposte a screening supportato dall’AI e 40.030 nel gruppo di controllo, che sono state sottoposte a doppia lettura standard. “Abbiamo rilevato che l’utilizzo dell’intelligenza artificiale ha portato alla rilevazione del 20% (41) di tumori in più rispetto allo screening standard, senza influire sui falsi positivi”, afferma Lång. Allo stesso tempo, il carico di lavoro per i radiologi è stato ridotto del 44%.
Anche l’aspetto temporale è importante: il numero di letture dello schermo con lo screening supportato dall’intelligenza artificiale è stato di 46.345 rispetto a 83.231 con lo screening standard. Lång spiega che, in media, un radiologo legge 50 esami di screening all’ora. I ricercatori hanno stimato che ci sono voluti circa cinque mesi in meno del tempo di un radiologo per leggere i circa 40.000 esami di screening nel gruppo AI.
“Lo studio – precisano gli autori – è stato condotto in un unico sito, in un ambiente svedese. Dovremo verificare ora se questi risultati promettenti reggono in altre condizioni, ad esempio con altri radiologi o altri algoritmi di intelligenza artificiale. Potrebbero esserci altri modi per utilizzare l’intelligenza artificiale nello screening mammografico, ma anche questi dovrebbero preferibilmente essere studiati in un contesto prospettico”.
I risultati provvisori hanno evidenziato che l’analisi delle mammografie del gruppo di intervento effettuata dall’IA insieme a uno o due radiologi rispetto alla lettura effettuata da due radiologi senza IA del gruppo di controllo ha portato all’individuazione del 20% di tumori in più, con un tasso di tumori individuati di 6,1 per mille partecipanti nel gruppo di intervento rispetto al tasso di 5,1 ogni mille donne del gruppo di controllo.
Nel gruppo di intervento è stata rilevata anche una significativa riduzione del carico di lavoro per i radiologi, che hanno dedicato il 44% in meno di tempo alla lettura delle mammografie, dal momento che la doppia lettura nel gruppo di intervento è stata riservata solo alle interpretazioni più critiche.
Venendo ai tassi di richiamo per ulteriori accertamenti, questi sono stati del 2,2% nel gruppo di intervento supportato dall’IA (244 donne) e del 2% nel gruppo di controllo (203 donne), portando all’individuazione di 41 tumori in più con il supporto dell’IA, dei quali 19 invasivi e 22 in situ.
IL COMMENTO
Nereo Segnan e Antonio Ponti del Centro di Riferimento per l’Epidemiologia e la Prevenzione Oncologica piemontese nel commentare in particolare i risultati preliminari dello studio MASAI sottolineano come il loro valore risieda indubbiamente nel risparmio di risorse ottenuto grazie alla riduzione del numero di seconde letture necessarie e nella capacità dell’algoritmo utilizzato dall’IA , peraltro molto accurato, di identificare il gruppo di donne a basso rischio (punteggio 1-7), in questo studio ha rappresentato il 76,2% della popolazione target e nel quale è stato individuato il 2,5% dei tumori (6 tumori sui 244 totali del gruppo di intervento). Il valore predittivo positivo dello screening in questo studio è stato del 50,0% nel gruppo di donne con il punteggio di rischio più alto (10), con 208 (85,2%) tumori rilevati in 2875 (7,2%) donne che hanno preso parte allo screening nel gruppo di intervento.
Tuttavia, secondo Segnan e Ponti la possibile presenza di sovradiagnosi (cioè il sistema che identifica i non tumori) o di sovrarilevazione di lesioni indolenti, come una porzione rilevante di carcinomi duttali in situ, dovrebbe indurre cautela nell’interpretazione dei risultati che altrimenti sembrerebbero decisamente a favore dell’uso dell’IA. Nello studio, rispetto allo standard di cura, l’IA ha identificato infatti una percentuale (anche se non significativa) decisamente più elevata di carcinomi in situ tra i tumori rilevati dallo screening: il 25% di tutti i tumori nel gruppo di intervento rispetto al 19% nel gruppo di controllo.
E ormai da decenni si dibatte se la scoperta di un carcinoma in situ, in particolare se classificato come a basso rischio, sia benefica o dannosa nello screening del tumore al seno.
Resta quindi un’importante domanda di ricerca: l’IA, se adeguatamente strutturata, sarà in grado di catturare caratteristiche biologiche rilevanti – o, in altre parole, la storia naturale della malattia – come la capacità dei tumori di crescere e diffondersi?
Cautela arriva anche dal primo autore dello studio MASAI (Lång) che afferma che i risultati provvisori sulla sicurezza “non sono sufficienti da soli per confermare che l’intelligenza artificiale è pronta per essere implementata nello screening mammografico”. Ancora, l’intelligenza artificiale viene sempre più utilizzata in contesti medici, ma c’è ancora una forte preoccupazione su come gli algoritmi vengono definiti e convalidati, nonché sul potenziale di bias e diagnosi eccessive. In questo contesto, l’UE sta pianificando una regolamentazione rigorosa sull’uso dell’intelligenza artificiale e l’EMA sta lavorando per valutare i rischi e i benefici della tecnologia per lo sviluppo di farmaci.
Gli strumenti di intelligenza artificiale sono il futuro dello screening mammografico?
Alicia Gallegos
Le mammografie di screening non evidenziano quasi un cancro al seno su otto. Le prime ricerche suggeriscono che l’intelligenza artificiale (AI) potrebbe colmare questo divario di rilevamento e migliorare notevolmente la diagnosi precoce della malattia. Ma rimangono domande sul modo migliore per incorporare l’IA negli screening e se è troppo presto per implementare la tecnologia.
Già, alcune cliniche di radiologia offrono l’analisi AI delle mammografie attraverso un metodo di costo aggiuntivo. Le pazienti che si sottopongono a mammografia possono consultare le strutture RadNet ed hanno la possibilità di un ulteriore screening AI delle loro immagini. RadNet, il più grande proprietario nazionale e operatore di centri di imaging diagnostico fixed-site negli Stati Uniti con più di 370 sedi, ha lanciato per la prima volta il suo programma di intelligenza artificiale nel nord-est. L’azienda ha ora lanciato il suo prodotto in tutte le regioni del paese.
Poiché l’IA non è rimborsata dagli assicuratori, i pazienti devono pagare una tassa out-of-pocket di IA “Le pratiche di RadNet hanno identificato più di 400 donne il cui cancro è stato trovato prima di quanto sarebbe stato se l’IA non fosse stata presente”, ha detto Greg Sorensen MD, chief science officer di RadNet.
Come funziona il programma di intelligenza artificiale di RadNet? Le pazienti che accedono alle strutture RadNet per la mammografia di screening vengono sottopostie a una mammografia 3D ad alta risoluzione che include l’uso della tecnologia del rilevatore a risoluzione 70 micron, ha affermato il dottor Sorensen. La mammografia viene esaminata da un radiologo qualificato con l’assistenza di due programmi di intelligenza artificiale certificati dalla Food and Drug Administration, Saige-Q e Saige-Density. Il radiologo fa poi un’interpretazione.
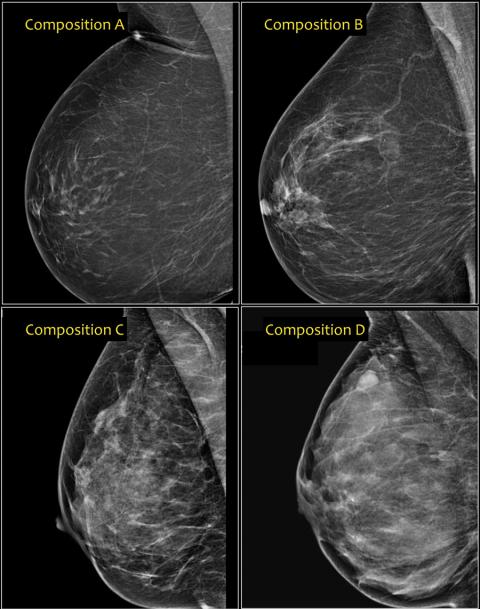
Saige-Q è uno strumento di intelligenza artificiale che aiuta a identificare mammografie più sospette fornendo un segnale rapido ai radiologi se l’IA considera una determinata mammografia in una categoria sospetta, secondo il dottor Sorensen. Saige-Density fornisce una valutazione di densità per ogni mammografia utilizzando una delle quattro categorie standard:
- A. Quasi interamente adiposo
- B. Aree sparse di densità fibroghiandolare
- C. Eterogeneamente denso
- D. Estremamente denso
A partire da settembre 2024, la FDA richiederà a tutti i rapporti mammografici di indicare la densità. Per i pazienti che scelgono il servizio aggiuntivo da 40 dollari, chiamato Enhanced Breast Cancer Detection, vengono applicati anche altri due programmi di intelligenza artificiale registrati dalla FDA: Saige-Dx e Saige-Assure. Questi programmi di intelligenza artificiale fanno un ulteriore passo avanti posizionando segni sulle aree all’interno delle immagini che trovano sospette. I mammogrammi contrassegnati come “alta sospetta” dall’IA vengono poi esaminati da un secondo radiologo umano. Il primo e il secondo radiologi conferiscono per concordare una diagnosi finale, ha spiegato il dottor Sorensen
“La nostra ricerca mostra che circa il 20% in più di tumori si trova quando il processo di revisione della salvaguardia è in atto”, ha detto il dottor Sorensen. “Abbiamo anche visto [30%] diminuzioni dei tassi di richiamo” – la percentuale di casi di screening in cui ulteriori test sono raccomandati dal radiologo.
La radiologa di Bethesda Janet Storella, MD, ha utilizzato il programma di intelligenza artificiale per circa 3 anni e ha affermato che la tecnologia ha migliorato le sue prestazioni di screening. L’IA è collegata al software di imaging della sua pratica e i radiologi hanno la possibilità di accendere l’IA in qualsiasi momento durante la lettura delle mammografie di screening, ha spiegato il dottor Storella. Alcuni radiologi esaminano prima la mammografia e poi avviano l’IA, mentre altri come il dottor Storella la accendono all’inizio, ha detto. Una volta avviata, l’IA disegna scatole di delimitazione – o delinea – intorno ad aree che ritiene sospette.
L’IA aiuta a focalizzare l’attenzione della dottoressa Storella su aree sospette e classifica il livello di sospetto in una delle quattro categorie: alto, intermedio, basso e minimo, ha detto. “Lo trovo particolarmente utile nelle pazienti che hanno tessuto mammario denso”, ha detto il dottor Storella, direttore medico dell’imaging femminile presso Community Radiology Associates, uno studio RadNet. “In queste situazioni, il tessuto sulla mammografia è un campo di bianco e anche i tumori sono bianchi, quindi stai cercando quella piccola palla da golf bianca su un mare di neve. L’IA aiuta davvero ad affarare questo in aree specifiche”.
Circa il 35% dei pazienti con mammografia di screening di RadNet si è iscritto al programma Enhanced Breast Cancer Detection, secondo i dati di RadNet. In un recente studio di nove radiologi generali e nove specialisti dell’imaging del seno, tutti i radiologi hanno migliorato le loro prestazioni interpretative delle mammografie di screening DBT quando leggevano con l’IA di RadNet vs senza di essa. (Un’area media sotto la curva caratteristica operativa del ricevitore [AUC] di 0,93 vs 0,87, che dimostra una differenza di AUC di 0,06 (IC 95%, 0,04-0,08; P < .001)
La mammografia è pronta per l’IA?
RadNet è tra un numero crescente di aziende commerciali che offrono soluzioni di intelligenza artificiale per la mammografia. MammoScreen e Hologic, ad esempio, sono altre due aziende che forniscono programmi di intelligenza artificiale per assistere i radiologi nella lettura delle mammografie di screening.
“Siamo all’inizio dell’integrazione dell’IA nell’imaging al seno a questo punto”, ha detto Laura Heacock, MD, radiologo di imaging al seno e professore associato di radiologia alla NYU Langone Health. “Ci sono più modelli di intelligenza artificiale commerciale ora disponibili per i radiologi da utilizzare nella loro pratica [e] probabilmente ce ne saranno altri. Siamo nella fase di transizione in cui le persone stanno ancora decidendo: qual è il modello migliore con cui andare? Come faccio a metterlo nel mio sistema? Come faccio a garantire che funzioni come previsto? Ogni pratica e sistema medico avrà una risposta diversa a questa domanda”.
Alla NYU Langone Health, i ricercatori hanno sviluppato e studiato modelli di intelligenza artificiale ottimali per l’imaging al seno per diversi anni, ha detto il dottor Heacock. I ricercatori, finora, hanno sviluppato modelli di intelligenza artificiale per la mammografia digitale 2D, le mammografie 3D, l’ecografia del seno e la risonanza magnetica del seno. Simile ai sistemi di intelligenza artificiale commerciali, l’IA è incorporata nel sistema di archiviazione e comunicazione delle immagini (PACS) utilizzato dai radiologi per rivedere le immagini. I radiologi premono un pulsante per avviare l’IA, che disegna una scatola intorno alle aree sospette dell’immagine e segna il sospetto.
“Do un’occhiata a dove si trova sulla mammografia e decido se si adatta al mio livello di sospetto”, ha detto il dottor Heacock. L’IA potrebbe non capire le cose sulla mammografia come facciamo noi. Per esempio, le cicatrici chirurgiche sembrano molto sospette per un modello di intelligenza artificiale. Ma se sto guardando una mammografia in cui [il paziente] ha avuto una cicatrice stabile che non è cambiata da 10 anni, non sono preoccupato che l’IA l’abbia trovata sospetta. Il mio giudizio clinico è l’ultimo decisore. Questa è solo un’informazione aggiuntiva che mi è utile”.
Una ricerca della New York University (NYU) ha dimostrato che quando vengono utilizzati da un radiologo esperto i modelli di intelligenza artificiale hanno migliorato il rilevamento del cancro al seno in tutte e quattro le modalità, ha detto.
Tuttavia, l’IA non è ancora stata lanciata alla NYU Langone. Sono necessarie ulteriori ricerche prima di implementare la tecnologia, secondo il dottor Heacock.
“Alla NYU, stiamo ancora testando i benefici per i pazienti”, ha detto. “Sappiamo che migliora il rilevamento del cancro, ma vogliamo assicurarci che non ci siano inconvenienti. Stiamo ancora esplorando i modi migliori per metterlo in atto nella nostra istituzione”.
Il dottor Heacock ha indicato recenti studi sull’IA nella mammografia di screening che mostrano promesse.
Un’analisi di oltre 80.000 donne, per esempio, pubblicata su The Lancet Oncology in agosto, ha scoperto che la lettura dello schermo supportata dall’IA ha portato a un tasso di rilevamento del cancro simile rispetto a un sistema di lettura per due persone. Questo screening ha portato a 244 tumori rilevati sullo schermo, 861 richiami e un totale di 46.345 letture dello schermo, secondo lo studio. Lo screening standard ha portato a 203 tumori rilevati dallo schermo, 817 richiami e un totale di 83.231 letture dello schermo.
Il sistema di intelligenza artificiale ha anche ridotto il carico di lavoro di lettura dello schermo per i radiologi del 44%, ha rilevato lo studio. Nel frattempo, uno studio del settembre 2023, pubblicato su The Lancet Digital Health, ha rilevato che la sostituzione di un radiologo con l’IA ha portato a un maggiore rilevamento del cancro senza un grande aumento dei casi falsi positivi. L’IA ha portato a un tasso di rilevamento del cancro non inferiore del 4% più alto rispetto alla doppia lettura del radiologo, secondo lo studio. Il dottor Heacock ha sottolineato che entrambi gli studi sono stati condotti in Europa, dove lo standard è per due radiologi per valutare le mammografie. “Questo rende i risultati entusiasmanti, ma non ancora direttamente applicabili alla pratica statunitense”, ha detto. Cosa consigliano gli esperti?
Stamatia V. Destounis, MD, FACR, presidente dell’American College of Radiology (ACR) Breast Imaging Commission, ha affermato che il college accoglie con favore la ricerca in corso sull’efficacia delle tecnologie di intelligenza artificiale e che l’IA può rivelarsi utile come strumento di flusso di lavoro migliorato. L’ACR non ha rilasciato alcuna guida sull’uso dell’IA per i radiologi e non ha alcuna raccomandazione sulle migliori pratiche, ha detto il dottor Destounis. “Le decisioni su quali tecnologie che vari sistemi sanitari e siti di radiologia scelgono di utilizzare sono prese da quelle strutture”, ha detto.
Il dottor Destounis ha affermato che sono necessarie ulteriori ricerche per dimostrare se le tecnologie di intelligenza artificiale aiutano o meno i radiologi a produrre risultati migliori nell’identificazione di malattie, lesioni e malattie tra la popolazione generale o in gruppi specifici, in base all’età, alle caratteristiche fisiche, alla razza, all’etnia o allo stato di rischio per il cancro al seno.
“Inoltre, è necessario un modo per misurare ogni prodotto di intelligenza artificiale in modo da poter essere certi che siano relativamente equivalenti nella loro efficacia e accuratezza – inizialmente e per un periodo di tempo prolungato”, ha detto.
Non esiste alcun consenso o raccomandazione concreta sull’uso dell’IA nello screening mammografico, aggiunge Peter P. Yu, MD, FACP, FASCO, medico capo presso l’Hartford HealthCare Cancer Institute e membro della nuova task force dell’IA della American Society of Clinical Oncology. Una delle tante discussioni riguardanti l’IA è in che misura i pazienti dovrebbero essere consapevoli che l’IA viene utilizzata nella loro assistenza sanitaria e se dovrebbero essere tenuti a dare il consenso al suo uso, ha detto il dottor Yu.
Se l’IA viene utilizzata per assistere i radiologi con l’interpretazione mammografica, i radiologi dovrebbero discutere con i pazienti come viene utilizzata e spiegare che la lettura finale è nelle mani del loro medico radiologo, ha detto.”Nella situazione improbabile in cui non c’era un essere umano nel giro e l’IA stava in effetti prendendo una decisione medica, il paziente deve essere consapevole”, ha detto. “Non sono consapevole che una situazione del genere esista oggi. È più probabile che l’IA sia sottilmente incorporata nel software che gestisce la tecnologia, proprio come è incorporata nella produzione e nel trasporto”.
Chi pagherà per l’IA?
Quando si tratta di pagamento, il dottor Yu ha affermato che spostare il costo dell’IA ai pazienti crea un rischio serio. “Ha un enorme potenziale per aumentare le disuguaglianze sanitarie”, ha detto. “Se crediamo che l’assistenza sanitaria sia un diritto umano fondamentale, l’IA dovrebbe andare a beneficio di tutti, non solo di coloro che possono permetterselo. L’assistenza sanitaria non dovrebbe essere un oggetto di lusso; se funziona, funziona per tutti”. In generale, la questione del pagamento per l’IA è ancora piuttosto “spinosa”, ha osservato il dottor Heacock. Attualmente, non c’è modo per i medici di richiedere un rimborso diretto per le letture AI delle mammografie.
Mentre la dottoressa Heacock dice di essere solidale con le aziende che dedicano tempo e sforzi significativi alla loro tecnologia di intelligenza artificiale, non pensa che far pagare i pazienti sia la soluzione giusta.”Sappiamo che molte donne hanno già difficoltà a pagare i servizi relativi alla mammografia e questo è solo un altro addebito per confonderle o che non possono pagare”, ha detto.
Il dottor Sorensen si aspetta che, in modo simile alla mammografia 3D, i pagatori alla fine copriranno la tecnologia AI di RadNet e che i pazienti non dovranno più pagare di tasca propria. Un vettore Blue Cross inizierà a coprire l’IA nell’aprile 2024, ha concluso.
Questo articolo è apparso originariamente su MDedge.com, parte della rete professionale Medscape.IA e previsione del rischio in mammografia
L’intelligenza artificiale potrebbe prevederne il rischio a 5 anni dalla mammografia
Lo screening del cancro al seno con la mammografia è tra i metodi più efficaci, oggi a disposizione, per individuare precocemente il cancro al seno, ovvero in una fase della malattia in cui il trattamento risulta più efficace. Di conseguenza, sottoporsi regolarmente a mammografie può abbassare significativamente il rischio di morire di cancro al seno. Tuttavia, rimane poco chiaro come prevedere con precisione quali donne svilupperanno il cancro al seno solo attraverso lo screening. Ed è proprio su questo punto che hanno voluto far luce gli studiosi dell’Università di Duke a Durham, Usa.
Secondo il team di scienziati statunitense, l’intelligenza artificiale potrebbe aiutare a prevedere il rischio di cancro al seno a cinque anni dalla mammografia. I ricercatori hanno sviluppato e testato uno strumento predittivo basato su IA chiamato AsymMirai. Secondo i dati della American Cancer Society, una donna su 8, ovvero circa il 13% della popolazione femminile, svilupperà un cancro al seno invasivo nella sua vita e 1 donna su 39 (il 3%) morirà a causa della malattia. Gli esperti hanno confrontato 210.067 mammografie da 81.824 pazienti nell’EMory BrEast imaging Dataset (EMBED) dal gennaio 2013 al dicembre 2020 utilizzando diversi modelli tra cu AsymMirai, dimostrandone l’accuratezza.
La ricerca potrebbe influenzare la frequenza delle mammografie
I risultati hanno anche confermato l’importanza clinica dell’asimmetria del seno e, di conseguenza, evidenziano che proprio questa asimmetria bilaterale potrebbe essere impiegata in futuro come marcatore di imaging per il rischio di tumore. “Poiché il ragionamento dietro le previsioni di AsymMirai è facile da capire, potrebbe essere un utile complemento per i radiologi nelle diagnosi e nella previsione del rischio di cancro al seno – spiega Jon Donnelly, prima firma della ricerca -. Possiamo, con sorprendente precisione, prevedere se una donna svilupperà il cancro nei prossimi 1-5 anni basandoci esclusivamente sulle differenze localizzate tra il tessuto del seno sinistro e destro”, precisa. “Questo potrebbe avere un impatto pubblico. Potrebbe, in un futuro non troppo lontano – conclude – influenzare la frequenza con cui le donne si sottopongono a mammografie”.
Una migliore previsione del rischio è un obiettivo di ricerca attivo perché è utile per lo sviluppo di strategie di screening personalizzato volte a ridurre contemporaneamente gli oneri finanziari e psicologici della mammografia di screening e a giustificare l’uso di imaging avanzato mirato e la cadenza della ripetizione della mammografia. AsynìmMirai, sviluppato dall’Università di Duke a Durham (Usa), sarebbe in grado di prevedere il rischio di tumore al seno a 5 anni dalla mammografia. Questo studio retrospettivo era conforme all’Health Insurance Portability and Accountability Act ed è stato approvato dalla commissione di revisione istituzionale. E’ stata sviluppata un’architettura neurale attorno alla asimmetria bilaterale. Mirai, è una rete neurale di apprendimento addestrata sullo screening delle mammografie di 56 786 pazienti per prevedere il rischio di cancro al seno a breve termine (fino a 5 anni). I risultati di Mirai sono stati convalidati esternamente sui dati di sette ospedali in tre continenti. Nello studio sono state incluse mammografie di screening (n = 210 067) di 81 824 pazienti (età media, 59,4 anni ± 11,4 [SD]). Per valutare la asimmetria bilaterale è stato proposto AsymMirai. AsymMirai è un’alternativa semplificata a Mirai che calcola il rischio utilizzando solo asimmetrie bilaterali localizzate. Lo scopo dello studio era (a) identificare se la asimmetria bilaterale come marcatore mammografico è alla base del modello di apprendimento ; (b) utilizzare la asimmetria bilaterale come marcatore di imaging per creare un modello semplificato, AsymMirai, con un processo di ragionamento intelligibile; (c) valutare entrambi i modelli per determinare se AsymMirai può approssimare le prestazioni di Mirai nella previsione del rischio di cancro al seno di 1-5 anni. I risultati dello studio hanno confermato l’importanza clinica legata all’asimmetria mammografica del seno, questa condizione potrebbe essere usata come marcatore di imaging per il rischio di tumore. Le differenze localizzate di densità tra i due seni possono prevedere se una donna svilupperà un tumore nei prossimi 1-5 anni. “Questo segna un nuovo capitolo nel campo dell’IA”, ha detto Freitas, autore di un editoriale che loda il nuovo documento. “Si rende l’IA più tangibile e comprensibile, migliorando così il suo potenziale di accettazione”.
Donnelly ha descritto AsymMirai come una versione più semplice, trasparente e più facile da usare di Mirai, un modello di intelligenza artificiale rivoluzionario che ha fatto notizia nel 2021 con la sua promessa di determinare con una precisione senza precedenti la probabilità che una paziente abbia il cancro al seno entro i prossimi 5 anni.
Mirai ha identificato fino al doppio delle future diagnosi di cancro rispetto al calcolatore di rischio convenzionale Tyrer-Cuzick. Tyrer-Cuzick e altri calcolatori di rischio a bassa Tyrer-Cuzick e altri calcolatori di rischio a bassa tecnologia utilizzano la storia personale e familiare per calcolare statisticamente il rischio. Mirai, d’altra parte, analizza innumerevoli bit di dati grezzi incorporati in una mammografia per decifrare i modelli che gli occhi di un radiologo potrebbero non catturare. Quattro immagini, tra cui due angoli di ogni seno, vengono inserite nel modello, che produce un punteggio compreso tra 0 e 1 per indicare il rischio della persona di contrarre il cancro al seno in 1, 3 o 5 anni. Ma anche i creatori di Mirai hanno ammesso di non sapere esattamente come si arriva a quel punteggio – un fatto che ha alimentato l’esitazione ed i dubbi tra i medici.
Il coautore dello studio Fides Schwartz, MD, un radiologo del Brigham and Women’s Hospital di Boston, Massachusetts, ha affermato che i ricercatori sono stati in grado di decifrare il codice sulla “scatola nera” di Mirai, scoprendo che i suoi punteggi sono stati in gran parte determinati valutando sottili differenze tra il tessuto mammario destro e il tessuto mammario sinistro.
Sapendo questo, il team di ricerca ha semplificato il modello per prevedere il rischio basato esclusivamente sulla “asimmetria bilaterale locale”. È nato quindi AsymMirai. Il team ha quindi utilizzato AsymMirai per guardare indietro a > 200.000 mammografie di quasi 82.000 pazienti. Hanno scoperto che funzionava quasi bene come il suo predecessore, assegnando un rischio più elevato a coloro che avrebbero sviluppato il cancro il 66% delle volte (rispetto al 71% di Mirai). Nei pazienti in cui ha notato la stessa asimmetria più anni di fila ha funzionato ancora meglio, con un 88% di possibilità di dare alle persone che avrebbero sviluppato il cancro in seguito un punteggio più alto rispetto a quelle che non l’avrebbero fatto.
“Abbiamo scoperto che possiamo, con una precisione sorprendentemente elevata, prevedere se una donna svilupperà il cancro nei prossimi 1-5 anni sulla base esclusivamente delle differenze localizzate tra il suo tessuto mammario sinistro e destro”, ha detto Donnelly. Schwartz immagina un giorno in cui i radiologi potrebbero usare il modello per aiutare a sviluppare strategie di screening personalizzate per i pazienti. I medici potrebbero consigliare a quelli con punteggi più alti di essere sottoposti a screening più spesso di quanto suggeriscano le linee guida, integrare le mammografie con una risonanza magnetica e tenere d’occhio i punti problematici identificati dall’IA. Per le persone a rischio davvero basso, d’altra parte, forse possiamo salvare loro un esame annuale che non è super piacevole e potrebbe non essere necessario”, ha detto Schwartz. Robert Smith, PhD, vicepresidente senior della scienza della diagnosi precoce del cancro presso l’American Cancer Society, ha osservato che l’IA è stata utilizzata per decenni per cercare di ridurre il carico di lavoro dei radiologi e migliorare le diagnosi.
“Ma l’IA non ha mai vissuto al massimo del suo potenziale”, ha detto Smith, “molto spesso perché veniva usata come stampella da radiologi inesperti che, invece di interpretare la mammografia e poi vedere cosa aveva da dire, hanno finito per lasciare che l’IA facesse la maggior parte del lavoro che, francamente, non era così accurato”. È fiducioso che le iterazioni più recenti e più sofisticate delle piattaforme di imaging medico IA (circa 18-20 modelli sono in fase di sviluppo) possano alla fine salvare la vita delle donne, in particolare nelle aree in cui i radiologi scarseggiano.
Ci vorrà molto tempo prima che i medici, o i loro pazienti, siano disposti a rischiare di posticipare una mammografia basata su un algoritmo.
Conclusioni
La mammografia può essere supportata da modelli di intelligenza artificiale, che eseguono una selezione delle pazienti, indicando agli specialisti solo le immagini che richiedono ulteriore attenzione ed approfondimento. Vi è, però, chi richiama una maggiore prudenza in questo orientamento della diagnostica, come per esempio la dottoressa Joann G. Elmore, docente presso la David Geffen School of Medicine dell’Università della California di Los Angeles (UCLA), e il dottor Christoph I. Lee, del Dipartimento di Radiologia della Scuola di Medicina dell’Università di Washington (Seattle), che su JAMA Health Forum hanno sottolineato che «senza un approccio più robusto alla valutazione e implementazione dell’intelligenza artificiale, data l’adozione senza sosta della tecnologia emergente nella pratica clinica, rischiamo di non riuscire a imparare dai nostri errori passati nella mammografia». Elmore e Lee si riferiscono alla rapida crescita dei sistemi CAD affiancati alla mammografia verificatasi venti anni fa. Questi sistemi, similmente all’intelligenza artificiale, possono individuare nell’immagine mammografica caratteristiche che indicano sospetto di presenza di carcinoma mammario. I due docenti ricordano che dieci anni dopo l’approvazione da parte della FDA dei sistemi CAD, si è concluso che questi non migliorano l’accuratezza diagnostica della mammografia nella pratica clinica routinaria.
Gli autori ottolineano che l’uso del CAD (Assistenza Diagnostica Computerizzata) aumenta la diagnosi di falsi positivi, soprattutto dei carcinomi intraduttali. Ora, lo stesso rischio potrebbe esistere esiste per l’implementazione dell’intelligenza artificiale. Nel loro editoriale gli autori indicano alcuni aspetti su cui ragionare e lavorare per evitare di commettere lo stesso errore fatto con i CAD, che ovviamente portano anche a un aumento della spesa sanitaria. Il primo punto riguarda l’interazione tra medico e risultati offerti dall’algoritmo: il rischio che vi siano errori di interpretazione esiste e deve essere tenuto in conto. Ad oggi tutti i sistemi C.A.D. tendono a sovrastimare la presenza di lesioni in quanto basate su algoritmi di rilevazione geometrica. La figura del medico radiologo è imprescindibile per la formulazione della corretta diagnosi, come dice l’acronimo, C.A.D. è un sistema di aiuto, prezioso, vantaggioso, ma pur sempre un aiuto, solo ed esclusivamente di supporto alla variabile diagnostica medica.
La FDA dovrebbe richiedere studi più solidi, basati su un numero maggiore di pazienti e che diano dimostrazione della reale utilità e vantaggio associati all’implementazione dell’intelligenza artificiale. Altrimenti, si rischia di sostenere solo la crescita tecnologica e favorire il consumismo sanitario, ma senza che questo possa apportare risultati migliori. Al momento la FDA richiede solo che il modello non dia esiti inferiori all’approccio umano. Non da ultimo, occorre valutare l’impatto dell’uso dell’intelligenza artificiale sulla medicina legale e sulla responsabilità professionale. Gli autori chiedono una legge nazionale su questi punti.
(Lo studio: Elmore JG, Lee CI. Artificial Intelligence in Medical Imaging. Learning From Past Mistakes in Mammography. JAMA Health Forum. 2022;3(2):e215207. doi:10.1001/jamahealthforum.2021.5207)
Vi è infatti un vuoto regolatorio a proposito di IA con rischi legali e responsabiltà professionale. Problematiche: Vuoto regolatorio, collaborazione con enti regolatori e sviluppatori, accettabilità radiologo, responsabiltà professionale, implicazioni professionali, eccessiva fiducia nella lettura automatizzata. L’uso dell’intelligenza artificiale nello screening mammografico presenta notevoli potenzialità nel migliorare sicurezza diagnostica ed esiti clinici per la paziente con una maggiore efficacia dello screening. Nel prossimo futuro le intelligenze artificiali ci aiuteranno a estrapolare sempre più informazioni dalle immagini, per una diagnostica migliore e più sicura in ogni campo.
A nostro giudizio questi sistemi di lettura della mammografia avranno il compito di supportare lo specialista, esistono infatti situazioni in cui la stanchezza o l’eccessivo carico di lavoro possono ridurre la precisione diagnostica di un essere umano. Le macchine, di contro, non risentono della stanchezza, un aspetto da non sottovalutare. Occorre lavorare sullo sviluppo e validazione di interfaccia che consenta al medico di poter interagire tra la sua capacità diagnostica a quella dell’intelligenza artificiale che deve essere solo uno strumento di supporto.
Parlando di intelligenza artificiale dobbiamo sempre chiederci se le macchine sostituiranno l’essere umano, ma, per quanto riguarda gli esami ecografici, l’interpretazione del clinico è ancora oggi imprescindibile. I software di intelligenza artificiale oggi più diffusi e disponibili sono ‘allenatì su migliaia di immagini d’archivio, ma non tengono conto di molti altri fattori che aiutano invece a stimare la pericolosità di un nodulo nel tessuto mammario. Informazioni come l’età della paziente o una familiarità per tumore al seno ci permettono di valutare meglio le singole situazioni, cosa che i software non possono fare. Migliori risultati si potranno avere dall’interazione del lavoro umano con la macchina. L’esperienza del clinico in senologia è ancora un fattore determinante. Pur nei loro attuali limiti, dunque, l’Intelligenza Artificiale può aiutarci a rendere un servizio più efficiente e più equo laddove vi siano lacune degli operatori, vuoi per mancanza di esperienza o per variabili tipicamente umane come la stanchezza, di cui i software non risentono. L’intelligenza artificiale ha il potenziale per migliorare l’accesso alla diagnostica senologica in aree remote e carenti di servizi di screening, può contribuire a snellire la burocrazia automatizzando le procedure, ma non sostituisce le competenze umane piuttosto le integra.
Ogni rivoluzione ha bisogno di essere regolamentata per essere affidabile ed etica. Purtroppo le regole arriveranno dopo le innovazioni. Chi gestisce ricerca ed innovazione sono strutture private. che hanno il potere di dettare l’agenda a stati e politica. E’ importante un aggiornamento normativo che mette al riparo la dignità umana e l’uguaglianza, purtroppo ci sarà pure chi non potrà disporre di cure e servizi migliori. L’Intelligenza artificiale è una sfida che non può essere trascurata. Le macchine però possono pure determinare dequalificazione, assenza di dialogo di relazione, sostituzione di competenza umana c’è da chiedersi che società vogliamo? L’IA dovrà essere uno strumento al servizio degli esseri umani.